Cho 10 gam ACO3 tác dụng với dung dịch HCl dư thì thu được 2,24 lít khí CO2 (đktc). Cấu hình electron của A là (biết A có số hạt proton bằng số hạt nơtron)
A. 1s22s22p6
B. 1s22s22p63s2
C. 1s22s22p63s23p4
D. [Ar]4s2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Có phản ứng: ACO 3 + 2 HCl → ACl 2 + CO 2 + H 2 O
⇒ n A C O 3 = n C O 2 = 0 , 1 ⇒ M A C O 3 = 10 0 , 1 = 100 ⇒ A = 40
Vì A có N = Z và Z + N = 40 nên Z = 20
Khi đó cấu hình electron của A là 1s22s22p63s23p64s2.

\(A_2CO_3+2HCl\rightarrow2ACl+CO_2+H_2O\\ n_{CO_2}=n_{A_2CO_3}=0,1\left(mol\right)\\ \Rightarrow M_{A_2CO_3}=\dfrac{13,8}{0,1}=138\\ \Rightarrow M_A=39\left(Kali\right)\\ Tacó:M_A=A=P_A+N_A=39\\ Mà:N_A=1,0526P_A\\ \Rightarrow P=19;N=20\\ \Rightarrow CHe:1s^22s^22p^63s^23p^64s^1\)

Đáp án C
Gọi số mol mỗi ion NH4+, K+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = 0,3 mol
mkết tủa= mBaCO3+ mBaSO4= 197z+233t= 43 suy ra t= 0,1 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol= 0,1
Định luật bảo toàn điện tích: x+y=2z+ 2t suy ra y= 0,1 mol
mmuối= (18x+ 39y+60z+96t).2= 49,8 gam

Đáp án C
+ Bản chất phản ứng: P 2 : 2 H + + C O 3 2 - H 2 O + C O 2 ↑ ⇒ n C O 3 2 - = n C O 2 = 0 , 1 P 1 : N H 4 + + O H - N H 3 ↑ + H 2 O B a 2 + + C O 3 2 - B a C O 3 ↓ B a 2 + + S O 4 2 - B a S O 4 ↓ ⇒ n N H 4 + = n N H 3 = 0 , 3 n B a C O 3 = n C O 3 2 - = 0 , 1 n B a S O 4 = ( 43 - 0 , 1 . 197 ) : 233 = 0 , 1 + B T Đ T t r o n g m ộ t n ử a X : n K + = 2 n S O 4 2 - + 2 n C O 3 2 - - n N H 4 + = 0 , 1 m m u ố i t r o n g X = 2 ( m N H 4 + + m K + + m S O 4 2 - + m C O 3 2 - ) = 49 , 8 g a m

\(n_{MgCO_3}=\dfrac{12,6}{84}=0,15\left(mol\right)\)
\(MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\)
0,15 0,15
\(V_{CO_2}=0,15.22,4=3,36\left(l\right)\)
--> A

Đáp án C
Bảo toàn nguyên tố cho cacbon ta có
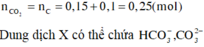
Thứ tự các phản ứng xảy ra khi cho từ từ dung dịch H+ vào dung dịch X là
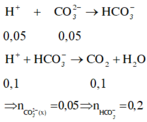
Các phản ứng tạo thành các chất trong dung dịch X
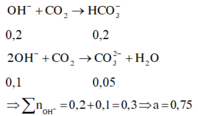
Có phản ứng:
Vì A có N = Z và Z + N = 40 nên Z = 20
Khi đó cấu hình electron của A là 1s22s22p63s23p64s2.
Đáp án D