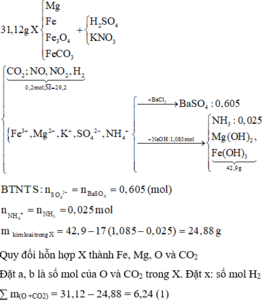
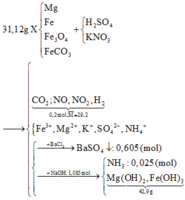
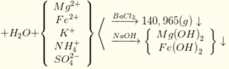
Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe, Fe3O4, FeCO3 vào dung dịch hỗn hợp chứa H2SO4 và KNO3. Sau phản ứng thu được 4,48 lít hỗn hợp khí Y (đktc) gồm (CO2; NO; NO2; H2) có tỉ khối hơi so với H2 là 14,6 và dung dịch Z chỉ chứa các muối trung hòa với tổng khối lượng là m gam. Cho BaCl2 dư vào Z thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác, cho NaOH dư vào Z thì thấy có 1,085 mol NaOH phản ứng đồng thời xuất hiện 42,9 gam kết tủa và 0,56 lít khí (đktc) thoát ra. Biết các phản ứng xảy ra hoàn toàn. Cho các nhận định sau:
(a) Giá trị của m là 82,285 gam.
(b) Số mol của KNO3 trong dung dịch ban đầu là 0,225 mol.
(c) Phần trăm khối lượng của FeCO3 trong X là 18,638%.
(d) Số mol của Fe3O4 trong X là 0,05 mol.
(e) Số mol Mg trong X là 0,15 mol
Số nhận định đúng là:
A. 4
B. 1
C. 3
D. 2


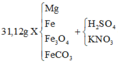
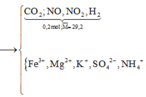
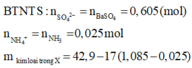 = 24,88 gam
= 24,88 gam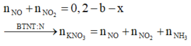

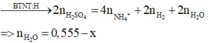
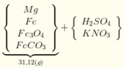
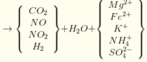
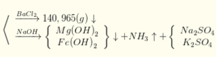
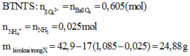
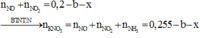
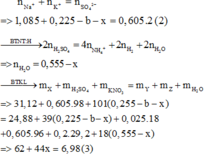
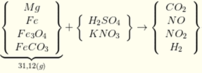
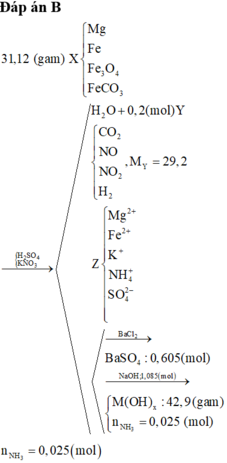
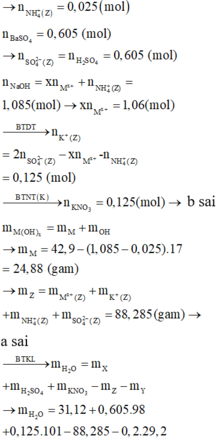
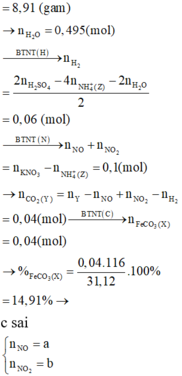
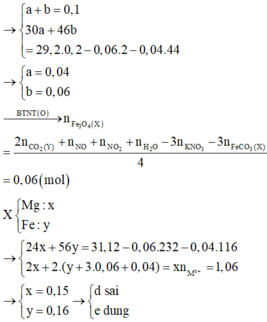
Đáp án B
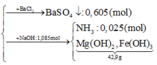
nSO42- = nBaSO4 = 0,605 mol
nNH4+ = nNH3 = 0,025 mol
=> m kim loại trong X = 42,9 - 17(1,085 - 0,025) = 24,88
Đặt a, b là số mol O và CO2 trong X. Đặt X là số mol H2.
=> 16a + 44b = 31,12 - 24,88 = 6,24 (1)
nNO + nNO2 = 0,2 - b - x
Bảo toàn N: nKNO3 = nNO + nNO2 + nNH3
=>nKNO3 = 0,225 -b-x
Sau phản ứng với NaOH thu được phần dung dịch chứa K2SO4 và Na2SO4, bảo toàn điện tích:
1,085 + 0,225 - b - x = 0,605.2 (2)
Bảo toàn H: 2nH2SO4 = 4nNH4+ + 2nH2 + 2nH2O
=>nH2O = 0,555 -x
Bảo toàn khối lượng:
31,12 + 0,605 . 98 + 101 (0,225 - b - x) = 24,88 + 39(0,225 - b - x) + 0,025.18 + 0,605.96 + 0,2.29,2 + 18(0,555 - x) (3)
Giải hệ (1)(2)(3):
a = 0,28
b = 0,04
b = 0,04 X = 0,06
m = 24,88 + 39(0,225 - b - x) + 0,025.18 + 0,605.96 = 88,285 => Nhận định a) sai
nKNO3 = 0,225 - b - X = 0,125 => Nhận định b) sai
%FeCO3 = 0,04.116/31,12= 14,91 % => Nhận định c) sai
nO = 4nFe3O4 + nFeCO3 => nFe3O4 = 0,06 => Nhận định d) sai