Hỗn hợp A gồm FeO, Fe3O4, Fe2O3. Trong hỗn hợp A, mỗi oxit đều có 0,5 mol. Khối lượng của hỗn hợp A là
A. 231 gam. B. 232 gam.
C. 233 gam. D. 234 gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B.
Có thể coi 0,5 mol FeO và 0,5 mol Fe2O3 là 0,5 mol Fe3O4. Vậy cả hỗn hợp có 1 mol Fe3O4 nên có khối lượng là 232g.

a,\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: x 2x
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: y 6y
Ta có: \(\left\{{}\begin{matrix}80x+160y=16\\2x+6y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
PTHH: CuO + 2HCl → CuCl2 + H2O
Mol: 0,1 0,2
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: 0,05 0,3
\(\Rightarrow m_{CuO}=0,1.80=8\left(g\right);m_{Fe_2O_3}=16-8=8\left(g\right)\)
b,\(\%m_{CuO}=\dfrac{8.100\%}{16}=50\%;\%m_{Fe_2O_3}=100-50=50\%\)

Câu 1 : a) \(n_{H_2}=\dfrac{13,2.10^{23}}{6.10^{23}}=2,2\left(mol\right)\)
Fe2O3 + 3H2 ----to---> 2Fe + 3H2O
Fe3O4 + 4H2 ----to---> 3Fe + 4H2O
Gọi x, y lần lượt là số mol Fe2O3 và Fe3O4
\(\left\{{}\begin{matrix}160x+232y=62,4\\3x+4y=2,2\end{matrix}\right.\)
Ra nghiệm âm, bạn xem lại đề câu này nhé
Sửa đề câu này số mol H2=1,1 (mol)
\(\left\{{}\begin{matrix}160x+232y=62,4\\3x+4y=1,1\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> \(\%m_{Fe_2O_3}=\dfrac{0,1.160}{62,4}=25,64\%\)
\(\%m_{Fe_3O_4}=100-25,64=74,36\%\)
b \(n_{Fe}=2x+3y=2.0,1+3.0,2=0,8\left(mol\right)\)
=> \(m_{Fe}=0,8.56=44,8\left(g\right)\)
Câu 2: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(Fe_2O_3+6HCl\rightarrow FeCl_3+3H_2O\) (2)
a) \(n_{H_2}=n_{Zn}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
\(n_{HCl\left(1\right)}=2n_{H_2}=0,12\left(mol\right)\)
=> \(n_{Fe_2O_3}=\dfrac{7,1-0,06.65}{160}=0,02\left(mol\right)\)
\(n_{HCl\left(2\right)}=6n_{Fe_2O_3}=0,12\left(mol\right)\)
=> \(m_{HCl}=\left(0,12+0,12\right).36,5=8,76\left(g\right)\)
b) CuO + H2 ----to---> Cu + H2O
Fe3O4 + 4H2 ----to---> 3Fe + 4H2O
Bảo toàn nguyên tố H :\(n_{H_2}.2=n_{H_2O}.2\)
=> \(n_{H_2O}=0,06\left(mol\right)\)
Bảo toàn khối lượng: \(m_{\left(Cu+Fe\right)}=m_{\left(CuO+Fe_3O_4\right)}+m_{H_2}-m_{H_2O}\)
=> \(m_{\left(Cu+Fe\right)}=3,92+0,06.2-0,06.18=2,96\left(g\right)\)

Đáp án D
Các phản ứng xảy ra:
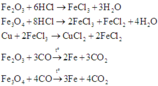
Nhận thấy: nO giảm = n O ( X ) = 1 2 n H C l = 0 , 5
⇒ a = m r ắ n s a u p h ả n ứ n g + m O g i ả m = 50 ( g a m )
Để tính được phần trăm khối lượng của Cu trong hỗn hợp X ta cần biết thêm khối lượng của Cu trong X.
Khi cho X vào dung dịch HCl dư thì chất rắn không tan còn lại sau phản ứng là Cu dư.
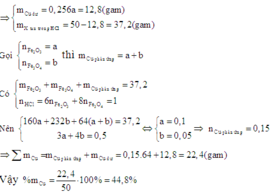
Có thể coi 0,5 mol FeO và 0,5 mol \(Fe_2O_3\) là 0,5 mol \(Fe_3O_4\)
Vậy cả hỗn hợp có 1 mol \(Fe_3O_4\) nên khối lượng là \(232\)g
Có thể coi 0,5 mol FeO và 0,5 mol Fe2O3Fe2O3 là 0,5 mol Fe3O4Fe3O4
Vậy cả hỗn hợp có 1 mol Fe3O4Fe3O4 nên khối lượng là 232232g