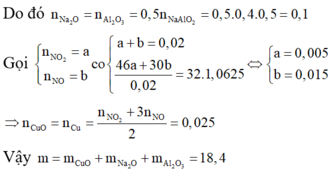Oxi hoá hoàn toàn 5,6l NH3 ( ở 0°C và 1530mmHg) có xúc tác thu được khí A, oxi hoá khí A thu được khí B có màu nâu đỏ, hoà tan B trong 146ml nước với sự có mặt của oxi thu được dd D. Tính nồng độ % của chất tan trong dd D.\(_{ }\)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


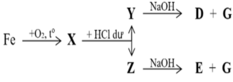
X + O2 ---> Oxit
BKTL => mO2 = 11,1 - 6,3 = 4,8 gam <=> nO2 = 0,15 mol
O20 + 4e --> 2O-2
0,15 --- 0,6
=> số mol electron do 6,3 gam X nhường là 0,6 mol
=> số mol electron do 12,6 gam X nhường là 0,6.2 = 1,2 mol
X + HCl --> muối clorua + H2
2H+1 + 2e --> H2
1,2 ---> 0,6 mol
V H2 = 0,6.22,4 = 13,44 lít

Td với H2SO4:
\(n_{H_2}=\dfrac{2,9748}{24,79}=0,12mol\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{Al}=\dfrac{0,12.2}{3}=0,08mol\)
Td với HNO3:
\(n_{Al}=a=0,08mol\\ n_{Cu}=b\)
Khí hoá nâu trong không khí → NO
\(n_{NO}=\dfrac{3,664}{24,79}=0,16mol\\ 3Cu+8HNO_3\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\\ Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO+2H_2O\)
\(\Rightarrow a+\dfrac{2}{3}b=0,16\\ \Leftrightarrow0,08+\dfrac{2}{3}b=0,16\\ \Leftrightarrow b=0,12mol\\ \Rightarrow m=0,08.27+0,12.64=9,84g\)

a) PTHH: \(Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO\uparrow+2H_2O\) (1)
\(10Al+36HNO_3\rightarrow10Al\left(NO_3\right)_3+3N_2\uparrow+18H_2O\) (2)
\(8Al+30HNO_3\rightarrow8Al\left(NO_3\right)_3+3NH_4NO_3+9H_2O\) (3)
b) Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{HNO_3\left(1\right)}=0,8\left(mol\right)\\n_{HNO_3\left(2\right)}=0,72\left(mol\right)\\n_{HNO_3\left(3\right)}=0,75\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(\left\{{}\begin{matrix}n_{NO}=0,2\left(mol\right)\\n_{N_2}=0,06\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{NO}=0,2\cdot22,4=4,48\left(l\right)\\V_{N_2}=0,06\cdot22,4=1,344\left(l\right)\end{matrix}\right.\)

a, \(n_{Ca}=\dfrac{12}{40}=0,3\left(mol\right)\)
PT: \(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
Theo PT: \(n_{H_2}=n_{Ca}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{Ca\left(OH\right)_2}=n_{Ca}=0,3\left(mol\right)\Rightarrow m_{Ca\left(OH\right)_2}=0,2.74=22,2\left(g\right)\)
c, \(n_{Fe_3O_4}=\dfrac{8,4}{232}=\dfrac{21}{580}\left(mol\right)\)
PT: \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
Xét tỉ lệ: \(\dfrac{\dfrac{21}{580}}{1}< \dfrac{0,3}{4}\), ta được H2 dư.
Theo PT: \(n_{Fe}=3n_{Fe_3O_4}=\dfrac{63}{580}\left(mol\right)\Rightarrow m_{cr}=m_{Fe}=\dfrac{63}{580}.56=\dfrac{882}{145}\left(g\right)\)

nFe = 16.8/56 = 0.3 (mol)
3Fe + 2O2 -to-> Fe3O4
0.3......0.2...........0.1
VO2 = 0.2*22.4 = 4.48 (l)
mFe3O4 = 0.1*232 = 23.2 (g)

\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{CuO}=n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right);n_{O_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ a,V_{O_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ V_{kk\left(đktc\right)}=\dfrac{100.1,12}{20}=5,6\left(l\right)\\ b,m_{CuO}=0,1.80=8\left(g\right)\\ c,2R+O_2\rightarrow\left(t^o\right)2RO\\ n_R=2.n_{O_2}=2.0,05=0,1\left(mol\right)\\ M_R=\dfrac{2,4}{0,1}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow R:Magie\left(Mg=24\right)\)

Đáp án D
Vì dung dịch D chỉ chứa một chất tan duy nhất và chất rắn G chỉ gồm một chất nên dung dịch D chứa NaAlO2 và G chứa CuO.