13/ Cho 3,6 gam kim loại M tác dụng vừa đủ với dung dịch chứa AgNO3 ,sau phản ứng thu được 32,4 gam một kim loại loại..Xác định M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)

Sau phản ứng thu được 2 kim loại là Ag và Cu => Mg và Al phản ứng hết.
Đặt số mol Cu2+ phản ứng là x
=> m + 57,8 = 108.0,5 + 64x
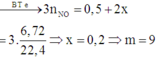
=> Chọn đáp án A

PTHH: \(4X+nO_2\underrightarrow{t^o}2X_2O_n\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Ta có: \(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\) \(\Rightarrow n_{O_2}=0,025\left(mol\right)\)
\(\Rightarrow n_{X_2O_n}=\dfrac{0,05}{n}\left(mol\right)\) \(\Rightarrow M_{X_2O_n}=\dfrac{3,1}{\dfrac{0,05}{n}}=62n\)
Ta thấy với \(n=1\) \(\Rightarrow M_{X_2O}=62\) \(\Rightarrow M_X=23\)
Vậy kim loại cần tìm là Natri

Gọi n là hóa trị của kim loại M
$n_{Ag} = \dfrac{32,4}{108} = 0,3(mol)$
$M + nAgNO_3 \to M(NO_3)_n + nAg$
Theo PTHH : $n_M = \dfrac{1}{n}n_{Ag} = \dfrac{0,3}{n}(mol)$
$\Rightarrow \dfrac{0,3}{n}.M = 3,6 \Rightarrow M = 12n$
Với n = 2 thì M = 24(Magie)