hợp chất B có vai trò trò cơ thể người để xác định hợp chất B người ta cho chất B tác dụng hết với kim loại nhôm thì thu được 6,675 g AlCl3 và 1.68 l h2 tìm cthh của B
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cho hợp chất \(B\) tác dụng hết với kim loại \(Al\) thu đc \(AlCl_3\) và \(H_2\)
\(\Rightarrow B\)là \(HCl\) đó có n.tố H, Cl ở sp
Thử lại thấy thoả mãn yêu cầu
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
(Không chắc lắm @@)

Do cho B tác dụng với Al tạo ra sản phấm chứa Al, Cl, H
=> CTHH: HxCly
\(n_{AlCl3}=\frac{6,675}{133,5}=0,05\left(mol\right)\); \(n_{H2}=\frac{1,68}{22,4}=0,075\left(mol\right)\)
Áp dụng định luật bảo toàn nguyên tố
=> \(n_{Cl\left(B\right)}=n_{Cl\left(AlCl3\right)}=0,05.3=0,15\left(mol\right)\)
=> \(n_{H\left(B\right)}=n_{H\left(H2\right)}=0,075.2=0,15\left(mol\right)\)
=> x:y = 0,15:0,15 = 1:1
=> CTHH: HCl

Do B tác dụng với Al tạo ra sp chứa Al , CL, H
\(\rightarrow\) CTHH tổng quát : HxCLy ( x, y nguyên dương tối giản )
\(n_{AlCl3}=\frac{6,675}{133,5}=0,05\left(mol\right)\)
\(n_{H2}=\frac{1,68}{22,4}=0,075\left(mol\right)\)
Áp dụng định luật bảo toàn nguyên tố , ta có
\(\rightarrow n_{Cl\left(B\right)}=n_{Cl\left(AlCl3\right)}=0,05.3=0,15\left(mol\right)\)
\(\rightarrow n_{H\left(B\right)}=n_{H\left(H2\right)}=0,075.2=0,15\left(mol\right)\)
Ta có: \(x:y=0,15:0,15=1:1\)
CTHH đúng là HCl

A tác dụng với dung dịch A g N O 3 trong amoniac tạo ra Ag; vậy A có chức anđehit.
0,2 mol anđehit kết hợp với hiđro phải tạo ra 0,2 mol ancol B có công thức R ( C H 2 O H ) x
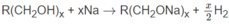
Theo phương trình 1 mol B tạo ra x/2 mol H 2
Theo đầu bài 0,2 mol B tạo ra 0,2 mol H 2
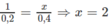
Vậy B là ancol hai chức và A là anđehit hai chức.
R ( C H O ) 2 + 4 A g N O 3 + 6 N H 3 + 2 H 2 O → R ( C O O N H 4 ) 2 + 4 N H 4 N O 3 + 4Ag↓
Số mol anđehit A = (x/4)số mol Ag 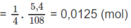
Khối lượng 1 mol A 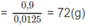
R ( C H O ) 2 = 72
⇒ R = 72 - 2.29 = 14. Vậy R là C H 2
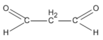 (propanđial)
(propanđial)

a)
\(n_{H_2\left(1\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2 (1)
0,6<----------------------0,3
=> mNa = 0,6.23 = 13,8 (g)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1<-0,2
=> mFe = 0,1.56 = 5,6 (g)
mCu = 10 (g)
\(\left\{{}\begin{matrix}\%Na=\dfrac{13,8}{13,8+5,6+10}.100\%=46,94\%\\\%Fe=\dfrac{5,6}{13,8+5,6+10}.100\%=19,05\%\\\%Cu=\dfrac{10}{13,8+5,6+10}.100\%=34,01\%\end{matrix}\right.\)
b)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,3}{y}\)<--0,3
=> \(M_{Fe_xO_y}=\dfrac{17,4}{\dfrac{0,3}{y}}=58y\left(g/mol\right)\)
=> 56x = 42y
=> \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4

a)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,6<----------------------0,3
Fe + 2HCl --> FeCl2 + H2
0,1<--0,2
=> \(\left\{{}\begin{matrix}m_{Na}=0,6.23=13,8\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Cu}=10\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Na}=\dfrac{13,8}{13,8+5,6+10}.100\%=46,94\%\\\%m_{Fe}=\dfrac{5,6}{13,8+5,6+10}.100\%=19,05\%\\\%m_{Cu}=\dfrac{10}{13,8+5,6+10}.100\%=34,01\%\end{matrix}\right.\)
b)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,3}{y}\)<--0,3
=> \(M_{Fe_xO_y}=56x+16y=\dfrac{17,4}{\dfrac{0,3}{y}}\left(g/mol\right)\)
=> \(\dfrac{x}{y}=\dfrac{3}{4}\)
=> CTHH: Fe3O4

