Nung hỗn hợp gồm bột nhôm và lưu huỳnh trong bình kín (không có không khí ) một thời gian được chất rắn A. Lấy chất rắn A cho vào dung dịch HCl dư, sau phản ứng thu được dung dịch B, chất rắn E, hỗn hợp khí F, còn nếu cho A vào dung dịch NaOH dư thu được dung dịch H, hỗn hợp khí F và chất rắn E. Dẫn F qua dung dịch Cu (NO3)2 dư, sau phản thu được kết tủa T, phần khí không hấp thụ vào dung dịch được dẫn qua ống chứa hỗn hợp MgO và CuO nung nóng thu được hỗn hợp chất rắn Q. Cho Q vào dung dịch H2SO4 loãng, dư thấy Q tan một phần, tạo thành dung dịch có màu xanh nhạt.
Hãy cho biết thành phần các chất có trong A, B, E, F, H, Q, T và viết các phương trình hóa học xảy ra .Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
Do khi hòa tan A vào HCl thu được hỗn hợp khí
=> Trong A chứa H2, H2S
=> Al dư, S hết
PTHH: 2Al + 3S --to--> Al2S3
0,2<--0,3------>0,1
2Al + 6HCl --> 2AlCl3 + 3H2
0,1----------------------->0,15
Al2S3 + 6HCl --> 2AlCl3 + 3H2S
0,1------------------------>0,3
=> \(\overline{M}_X=\dfrac{0,15.2+0,3.34}{0,15+0,3}=\dfrac{70}{3}\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{\dfrac{70}{3}}{2}=\dfrac{35}{3}\)

Fe + S -----> FeS
FeS + 2 HCl ----> FeCl2 + H2S
Fe + 2HCl ----> FeCl2 + H2
a) n(Fe) = 5,6 : 56 = 0,1 ( mol)
n ( S ) = 1,5 : 32 = 0,05 ( mol )
=> sau phản ứng thứ nhất : n(Fe) dư = 0,1 - 0,05 = 0,05 mol ; n(FeS) =n (S ) = 0,05 ( mol)
a) Các chất rắn trong B là: Fe và FeS
Các chất trong dung dịch A là : FeCl2 và HCl dư
b) n(H2 S) = n ( FeS ) = 0,05 ( mol) => V( H2S) = 0,05 x 22,4 = 1,12 ( lit)
n (H2 ) = n(Fe dư) = 0,05 ( mol ) => V( H2) = 1,12 ( lit)

Nung hỗn hợp BaCO3, Cu, FeO chỉ có BaCO3 bị nhiệt phân hủy
BaCO3 → t ∘ BaO + CO2↑ (B)
Rắn A gồm: Cu, FeO, BaO, có thể có BaCO3 dư
Khí B là CO2
CO2 + KOH → KHCO3
CO2 + 2KOH → K2CO3 + H2O
Dung dịch C gồm KHCO3 và K2CO3
KHCO3 + NaOH → K2CO3 + Na2CO3 + H2O
K2CO3 + CaCl2 → CaCO3↓ + 2KCl
A + H2O dư có phản ứng xảy ra:
BaO + H2O → Ba(OH)2
Vây dd D là Ba(OH)2
rắn E là Cu, FeO, có thể có BaCO3 dư
E + HCl dư → khí B + dd F + rắn G
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
FeO + 2HCl → FeCl2 + H2O
Dd F gồm: BaCl2, FeCl2 và HCl dư
Rắn G là Cu
A + H2SO4 đặc => hỗn hợp khí H ( từ đây khẳng định chắc chắn A có BaCO3 dư)
BaCO3 + H2SO4 đặc → t ∘ BaSO4↓ + CO2 + H2O
Cu + 2H2SO4 đặc → t ∘ CuSO4 + SO2↑ + 2H2O
2FeO + 4H2SO4 đặc → t ∘ Fe2(SO4)3 + SO2 + 4H2O
Hỗn hợp khí H gồm: SO2 và CO2
Dung dịch I gồm: CuSO4, Fe2(SO4)3, H2SO4 đặc, nóng dư
Kết tủa K là: BaSO4.

\(Fe+S-t^0->FeS\\ n_{Fe}:n_S=\dfrac{11,2}{56}:\dfrac{4,8}{32}=0,2:0,15\Rightarrow Fe:dư\left(0,05mol\right)\\ Fe+2HCl->FeCl_2+H_2\\ FeS+2HCl->FeCl_2+H_2S\\ d_{\dfrac{B}{kk}}=\dfrac{\dfrac{0,05.2+0,15.34}{0,2}}{29}=0,89655\)

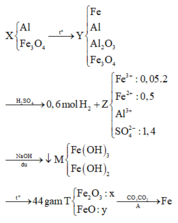
Khi cho A qua T thì khối lượng chất khí tăng chính là khối lượng O trong T → 16. ( 3x + y) = 0,208.50 →3x + y = 0,65

Đáp án C

- Chất rắn không tan trong HCL dư là S => m S dư = 3,8g
Kết tủa đen là CuS => n CuS = 0,1 = n H 2 S = nS phản ứng
m S phản ứng = 3,2g
0,2 mol Z gồm 0,1 mol H 2 S và 0,1 mol H 2
m ban đầu = 3,8 + 3,2 = 7g
Ta lại có
n Fe p / u = n S p / u = 0,1 mol
n Fe dư = n H 2 = 0,1 mol
n Fe ban đầu → m Fe ban đầu = 0,2 .56 = 1,12 g
Vậy m = 11,2 + 0,7 = 18,2 (gam)



2Al+3S----->Al2S3
Chất rắn A là Al2S..Có thể có Al dư hoặc S dư
Cho A vào HCl
Al2S3+6HCl--->2AlCl3+3H2S
2Al+ 6HCl---->2AlCl3+3H2
dd B là AlCl3 , có thể có HCl dư
Chất rắn E là S
Khí F là H2S và H2
Cho A vào NaOH
2Al+2NaOH+2H2O--->2NaAlO2+3H2
Al2O3+2NaOH--->2NaAlO2+H2O
đd H là NaAlO2 ,có thể có NaOH dư
Khí F là H2
Chất rắn E là S
Cho F vào Cu(NO3)2
H2S+Cu(NO3)2---->CuS+2HNO3
Kết tủaT là CuS
Khí k hấp thụ ch qua MgO và CuO
CuO+H2--->Cu+H2O
Chất rắn Q là MgO và Cu và CuO dư
Cho Q vào H2SO4
MgO+H2SO4----> MgSO4+H2O
CuO+H2SO4---->CuSO4(xanh nhạt)+H2O
@Cù Văn Thái xem hộ e vs