cho 1 mol N2 tác dụng với lượng H2 dư thì thu được 1,5 mol NH3 . Tính hiệu suất của phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
![]()
Do 1 1 > 4 3 → Hiệu suất tính theo N 2
Đặt số mol N2 ban đầu là x mol
→ nH2 ban đầu= 4x mol;
Do hiệu suất phản ứng là 25% nên
nN2 pứ= 25%.x= 0,25x mol
![]()
Ban đầu x 4x mol
Phản ứng 0.25x 0.75x 0.5x mol
Sau pứ 0.75x 3.25x 0.5x mol
Sau phản ứng nNH3= 0,5x= 1,5 suy ra x=3 mol
→V= 22,4. (x+3x)= 22,4.4.3=268,8 lít

Chọn C
Giả sử phản ứng xảy ra với H = 100% → N 2 hết →Hiệu suất tính theo N 2 .
Đặt số mol N 2 ban đầu là x mol, n N 2 ban đầu = 4x mol;
Do hiệu suất phản ứng là 25% nên n N 2 pứ = 25%.x = 0,25x mol
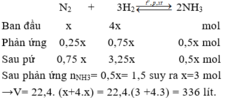

C
N2+3 H2 -> 2 NH3
0.2 0.6 0.4
x 3x 2x
x+3x+2x=0.6
x=0.1
H=(0.1*2)*100/0.4=50%

Câu 1 câu 2 giống nhau nên tui làm câu 1 thôi nha
\(N_2+3H_2\rightarrow2NH_3\)
\(H=20\%\Rightarrow n_{N_2}=2.0,2=0,4\left(mol\right);n_{H_2}=6.0,2=1,2\left(mol\right)\)
=> Tính theo N2
\(\Rightarrow m_{NH_3}=2.n_{N_2}.17=13,6\left(g\right)\)
3/ \(N_2+3H_2\rightarrow2NH_3\)
\(V--3V--2V\)
Thể tích còn lại sau phản ứng bao gồm N2 dư, H2 dư và NH3
\(\Rightarrow V_{N_2}-V+V_{H_2}-3V+2V=16,4\Rightarrow V=0,8\left(l\right)\) \(\Rightarrow V_{NH_3}=2.0,8=1,6\left(l\right)\)
\(\Rightarrow H=\frac{V}{V_{N_2}}=\frac{0,8}{4}=20\%\)
cho 1,86g hỗn hợp kim loại Mg và Al vào dung dịch HNO3 loãng , dư thì thu được 560ml khí N2O (đktc)
a. Viết phương trình phản ứng xảy ra
b. Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu

Đáp án : C
Saccarozo -> Glucozo + Fructozo
0,02.75% -> 0,015 -> 0,015 mol
Mantozo -> 2Glucozo
0,01.75% -> 0,015 mol
Vạy sau thủy phân có : 0,03 mol glucozo ; 0,015 mol fructozo và 0,0025 mol mantozo có thể phản ứng tráng bạc
=> nAg = 2(nGlucozo + nFructozo + nmantozo) = 0,095 mol

PTHH: \(N_2+3H_2\xrightarrow[xt]{t^o}2NH_3\)
Theo PTHH: \(n_{NH_3\left(lý.thuyết\right)}=2n_{N_2}=2\left(mol\right)\) \(\Rightarrow H\%=\dfrac{1,5}{2}\cdot100\%=75\%\)