Bài 2 : Hãy tính khối lượng phân tử của
a. 9,03 nhân 1023 phân tử CuSO4
b. 6,02 nhân 1023 phân tử N2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Bài 2 : Hãy tính khối lượng phân tử của
a. 9,03 nhân 1023 phân tử CuSO4
b. 6,02 nhân 1023 phân tử N2


Khối lượng bằng gam của:
- 6,02. 10 23 phân tử nước: 6,02. 10 23 .18.1,66. 10 - 24 = 17,988(g) ≈ 18(g)
- 6,02. 10 23 phân tử C O 2 : 6,02. 10 23 .44.1,66. 10 - 24 = 43,97(g) ≈ 44(g).
- 6,02. 10 23 phân tử C a C O 3 : 6,02. 10 23 .100. 1,66. 10 - 24 = 99,9(g) ≈ 100(g).

Số mol khí: n = N/ N A (N là số phân tử khí)
Mặt khác n = m/ μ . Do đó: μ = m N A /N = 15.6,02. 10 23 /5,46. 10 26 = 16,01. 10 - 3 (kg/mol) (1)
Trong các khí có hidro và cacbon thì C H 4 có:
μ = (12 + 4). 10 - 3 kg/mol (2)
So sánh (2) với (1) ta thấy phù hợp. Vậy khí đã cho là C H 4
Khối lượng của phân tử hợp chất là: m C H 4 = m/N
Khối lượng của nguyên tử hidro là:
m H 4 = 4/16 . m C H 4 = 4/16 . m/N ≈ 6,64. 10 - 27 (kg)
Khối lượng nguyên tử cacbon là:
m C = 12/16 . m C H 4 = 12/16 . m/N ≈ = 2. 10 - 26 (kg)

24.
10
23
phân tử
H
2
O
=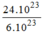 = 4(mol) phân tử
H
2
O
= 4(mol) phân tử
H
2
O
1,44.
10
23
phân tử
C
O
2
=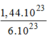 = 0,24(mol) phân tử
C
O
2
.
= 0,24(mol) phân tử
C
O
2
.
0,66.
10
23
phân tử
C
12
H
22
O
11
=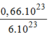 = 0,11(mol) phân tử
C
12
H
22
O
11
.
= 0,11(mol) phân tử
C
12
H
22
O
11
.

\(a_1,m_{CaCO_3}=0,25.100=25(g)\\ a_2,m_{SO_2}=\dfrac{3,36}{22,4}.64=9,6(g)\\ a_3,m_{H_2SO_4}=\dfrac{9.10^{23}}{6.10^{23}}.98=147(g)\)

Chọn D
A. 6. 10 23 phân tử H 2 = 1 mol H 2 ⇒ m H = 1.2 = 2g
B. 3. 10 23 phân tử H 2 O = 0,5 mol H 2 O ⇒ n H = 2. n H 2 O = 2. 0,5 = 1 mol ⇒ m H = 1.1 = 1g
C. 0,6 g C H 4 ⇒ n C H 4 = 0,6/16 = 0,0375 mol ⇒ n H = 4. n C H 4 = 0,0375 . 4 = 0,15 mol ⇒ m H = 1. 0,15 = 0,15 g
D. 1,5g N H 4 C l ⇒ n N H 4 C l = 1,5/53,5 = 0,028 mol ⇒ n H = 4. n C H 4 C l = 4. 0,028 = 0,112 mol ⇒ m H = 1. 0,112 = 0,112 g
Vậy trong N H 4 C l khối lượng hidro có ít nhất.

\(1.m_{Cu}=1,2.64=76,8\left(g\right)\\ 2.m_{NaCl}=1,25.58,5=73,125\\ 3.n_{C_6H_{12}O_6}=\dfrac{7,2.10^{23}}{6.10^{23}}=1,2\left(mol\right)\\ \Rightarrow m_{C_6H_{12}O_6}=1,2.180=216\left(g\right)\\ 4.n_{O_2}=3,6.32=115,2\left(g\right)\\ 5.n_{O_2}=\dfrac{1,2.10^{23}}{6.10^{23}}=0,2\left(mol\right)\\ \Rightarrow m_{O_2}=0,2.32=6,4\left(g\right)\\ 6.n_{N_2}=\dfrac{26,88}{22,4}=1,2\left(mol\right)\\ \Rightarrow m_{N_2}=1,2.28=33,6\left(g\right)\\ 7.n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ \Rightarrow m_{CO_2}=0,5.44=22\left(g\right)\\ 8.n_{H_2}=\dfrac{31,36}{22,4}=1,4\left(mol\right)\\ \Rightarrow m_{H_2}=1,4.2=2,8\left(g\right)\)
\(1,m_{Cu}=1,2\cdot64=76,8\left(g\right)\\ 2,m_{NaCl}=1,25\cdot58,5=73,125\left(g\right)\\ 3,n_{C_6H_{12}O_6}=\dfrac{7,2\cdot10^{-23}}{6\cdot10^{-23}}=1,2\left(mol\right)\\ \Rightarrow m_{C_6H_{12}O_6}=1,2\cdot180=216\left(g\right)\\ 4,m_{O_2}=3,6\cdot32=115,2\left(g\right)\\ 5,n_{O_2}=\dfrac{1,2\cdot10^{-23}}{6\cdot10^{-23}}=0,2\left(mol\right)\\ \Rightarrow m_{O_2}=0,2\cdot32=6,4\left(g\right)\\ 6,n_{N_2}=\dfrac{26,88}{22,4}=1,2\left(mol\right)\\ \Rightarrow m_{N_2}=1,2\cdot28=33,6\left(g\right)\\ 7,n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ \Rightarrow m_{CO_2}=0,5\cdot44=22\left(g\right)\\ 8,n_{H_2}=\dfrac{31,36}{22,4}=1,4\left(mol\right)\\ \Rightarrow m_{H_2}=1,4\cdot2=2,8\left(g\right)\)

Câu 1
\(m_{HNO_3}=0,3.63=18,9\left(g\right)\)
\(m_{CuSO_4}=1,5.160=240\left(g\right)\)
\(m_{AlCl_3}=2.133,5=267\left(g\right)\)
Câu 2
a) \(V_{N_2}=3.22,4=67,2\left(l\right)\)
\(V_{H_2}=0,45.22,4=10,08\left(l\right)\)
\(V_{O_2}=0,55.22,4=12,32\left(l\right)\)
b) \(V_{hh}=\left(0,25+0,75\right).22,4=22,4\left(l\right)\)

Cứ 1 mol chất là lượng chất có chứa 6. 10 23 phân tử (nguyên tử).
Vậy cứ 0,6. 10 23 phân tử các chất là số phân tử có trong 0,1 mol chất.
Khối lượng các chất là:
m C O 2 = n C O 2 . M C O 2 = 0,1.44 = 4,4(g)
m H 2 O = n H 2 O . M H 2 O = 0,1.18 = 1,8(g)
m O 2 = n O 2 . M O 2 = 0,1.32 = 3,2(g)
m H 2 = n H 2 . M H 2 = 0,1.2 = 0,2(g)
m N a C l = n N a C l . M N a C l = 0,1.58,5 = 5,85(g)

\(a.\)
\(n_{O_2}=\dfrac{0.15\cdot N}{N}=0.15\left(mol\right)\)
\(m_{O_2}=0.15\cdot32=48\left(g\right)\)
\(V_{O_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(b.\)
\(n_{CO_2}=\dfrac{1.44\cdot10^{23}}{6\cdot10^{23}}=0.24\left(mol\right)\)
\(m_{CO_2}=0.24\cdot44=10.56\left(g\right)\)
\(V_{CO_2}=0.24\cdot22.4=5.376\left(l\right)\)
\(c.\)
\(m_{H_2}=0.25\cdot2=0.5\left(g\right)\)
\(V_{H_2}=0.25\cdot22.4=5.6\left(l\right)\)
\(d.\)
\(m_{CH_4}=1.5\cdot16=24\left(g\right)\)
\(V_{CH_4}=1.5\cdot22.4=33.6\left(l\right)\)
\(e.\)
\(n_{CO_2}=\dfrac{8.8}{44}=0.2\left(mol\right)\)
\(V_{CO_2}=0.2\cdot22.4=4.48\left(l\right)\)
a) \(n_{CuSO_4}=\dfrac{9,03\times10^{23}}{6\times10^{23}}=1,505\left(mol\right)\)
\(\Rightarrow m_{CuSO_4}=1,505\times160=240,8\left(g\right)\)
b) \(n_{N_2}=\dfrac{6,02\times10^{23}}{6\times10^{23}}=\dfrac{301}{300}\left(mol\right)\)
\(\Rightarrow m_{N_2}=\dfrac{301}{300}\times28=28,093\left(g\right)\)