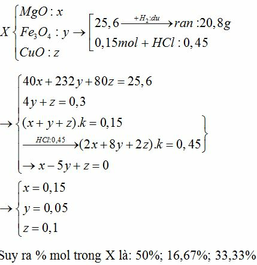Hỗn hợp X gồm FeO và CuO . Chia hỗn hợp X thành hai phần bằng nhau . Phần 1 phản ứng vừa đủ với dung dịch axit \(H_2SO_4\) có chưa 39,2 gam \(H_2SO_4\) . Cho phần 2 vào ống sứ , đốt nóng và dẫn 1 dòng khí CO đi qua ống . Sau phản ứng thấy trong ống còn lại 28gam hỗn hợp Y gồm 4 chất rắn và 10,2 gam khí đi ra khỏi ống . Cứ 1 lít khí này nặng gấp 1,275 lần 1 lít khí Oxi ( ở đktc) . Tính thành phần % khối lượng mỗi chất trong hỗn hợp X .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Gọi: \(\left\{{}\begin{matrix}n_{FeO}=a\left(mol\right)\\n_{CuO}=b\left(mol\right)\end{matrix}\right.\) (trong 1 phần)
- Phần 1: \(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
Ta có: \(n_{H_2SO_4}=0,2.2=0,4\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{FeO}+n_{CuO}=a+b=0,4\left(1\right)\)
- Phần 2: Khí thoát ra khỏi ống gồm CO dư và CO2.
Ta có: \(M_{hhk}=1,275.32=40,8\left(g/mol\right)\)
\(\Rightarrow n_{hhk}=n_{CO\left(dư\right)}+n_{CO_2}=\dfrac{10,2}{40,8}=0,25\left(mol\right)\)
BTNT C, có: nCO = nCO (dư) + nCO2 = 0,25 (mol)
Theo ĐL BTKL, có: mFeO + mCuO + mCO = mK + mhhk
⇒ 72a + 80b + 0,25.28 = 28 + 10,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
Do chia A thành 2 phần bằng nhau nên %m mỗi chất trong từng phần cũng là %m mỗi chất trong A.
\(\Rightarrow\left\{{}\begin{matrix}\%m_{FeO}=\dfrac{0,1.72}{0,1.72+0,3.80}.100\%\approx23,08\%\\\%m_{CuO}\approx76,92\%\end{matrix}\right.\)
b, Để thu được VH2 tối đa thì mFe (trong K) phải tối đa.
Ta có: \(\left\{{}\begin{matrix}n_{CO\left(dư\right)}+n_{CO_2}=0,25\\28n_{CO\left(dư\right)}+44n_{CO_2}=10,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{CO_{\left(dư\right)}}=0,05\left(mol\right)\\n_{CO_2}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ nFe max = nFeO = nO (trong FeO) = nCO2 = 0,2 (mol)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow n_{H_2\left(max\right)}=n_{Fe\left(max\right)}=0,2\left(mol\right)\Rightarrow V_{H_2\left(max\right)}=0,2.22,4=4,48\left(l\right)\)

Giả sử trong mỗi phần có: \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\\n_{Zn}=c\left(mol\right)\\n_O=d\left(mol\right)\end{matrix}\right.\)
=> 56a + 64b + 65c + 16d = 32,21
P1:
nO = nH2O = d (mol)
=> nHCl = 2d (mol)
Theo ĐLBTKL: mrắn bđ + mHCl = mmuối + mH2O
=> 32,21 + 73d = 59,16 + 18d
=> d = 0,49 (mol)
P2:
Gọi số mol HCl, H2SO4 là a, b (mol)
nH2O = nO = 0,49 (mol)
Bảo toàn H: a + 2b = 0,98 (1)
Theo ĐLBTKL: mrắn bđ + mHCl + mH2SO4 = mmuối + mH2O
=> 32,21 + 36,5a + 98b = 65,41 + 0,49.18
=> 36,5a + 98b = 42,02 (2)
(1)(2) => a = 0,48 (mol); b = 0,25 (mol)
=> \(\left\{{}\begin{matrix}C_{M\left(HCl\right)}=\dfrac{0,48}{1}=0,48M\\C_{M\left(H_2SO_4\right)}=\dfrac{0,25}{1}=0,25M\end{matrix}\right.\)

Đáp án B
· Phần 1: n Al = a 2 = n NaOH ⇒ a = 0 , 08 mol .
· Phần 2: Đặt số mol Cr2O3 trong 1 2 X phản ứng là x.
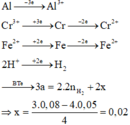
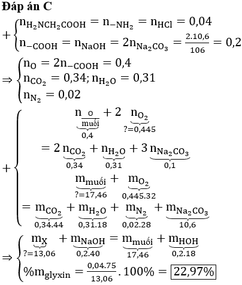
Þ Phần trăm khối lượng Cr2O3 chưa phản ứng = 0 , 03 - 0 , 02 0 , 03 . 100 % = 33 , 33 %