1. Ngâm một vật bằng đồng có khối lượng 15g trong 340g dd AgNO3 6%. Sau một thời gian lấy vật ra thấy khối lượng AgNO3 trong dung dịch giảm 25%. Tính khối lượng của vật sau phản ứng?
2. Cho 1,96g bột sắt vào 100ml dd CuSO4 10% có khối lượng riêng là 1,12g/ml
a)Viết ptpư
b) Xác định nồng độ mol/lit của các chất trong dd sau khi pư kết thúc
c) Cô cạn dd thu được bao nhiêu gam muối khan
3. Ngâm 1 lá sắt có khối lượng 28g trong dd đồng sunfat dư. Sau một thời gian lấy lá kẽm ra khỏi dd muối CuSO4 và đem cân thấy khối lượng của lá là 29,6g
a) Viết ptpư
b) Tính khối lượng sắt đã tham gia pư và khối lượng đồng tạo thành
4. Ngâm 1 lá Mg có khối lượng 24g trong dd sắt (II) clorua dư. Sau một thời gian lấy lá kẽm ra khỏi dd muối FeCl2 và đem cân thấy khối lượng của lá là 36,8g
a) Viết ptpư
b) Tính khối lượng Mg đã tham gia pư và khối lượng sắt tạo thành
c) Tính % khối lượng của Mg và sắt trong lá trên
d) Đem hòa tan 36,8g lá trên vào dd HCl dư. Tính thể tích khí thoát ra (đktc)
e) Đem hòa tan 36,8g lá trên vào dd HNO3 đặc dư. Tính thể tích khí thoát ra (đktc)

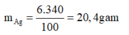
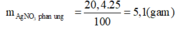
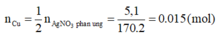

2. Cho 1,96g bột sắt vào 100ml dd CuSO4 10% có khối lượng riêng là 1,12g/ml
a)Viết ptpư
b) Xác định nồng độ mol/lit của các chất trong dd sau khi pư kết thúc
c) Cô cạn dd thu được bao nhiêu gam muối khan
---------
nFe= 1,96/56= 0,035(mol)
mddCuSO4= 100.1,12= 112(g)
=> mCuSO4= (112.10)/100= 11,2(g)
=> nCuSO4= 11,2/160= 0,07(mol)
PTHH: Fe + CuSO4 -> FeSO4 + Cu
Ta có: 0,035/1 < 0,07/1
=> Fe hết, CuSO4 dư, tính theo nFe
=> dd sau phản ứng gồm dd FeSO4 và dd CuSO4 dư.
Ta có: nCuSO4(p.ứ)= nFeSO4= nFe= 0,035(mol)
=> nCuSO4(dư)= 0,07 - 0,035= 0,035(mol)
Vddsau= VddCuSO4= 100(ml)= 0,1(l)
=> \(C_{MddCuSO_4\left(dư\right)}=\dfrac{0,035}{0,1}=0,35\left(M\right)\)
\(C_{MddFeSO_4}=\dfrac{0,035}{0,1}=0,35\left(M\right)\)
- Cô cạn dd dc 2 loại muối khan: CuSO4 (dư) và FeSO4.
m(muối_khan)= mCuSO4+ mFeSO4= 0,035.160 + 0,035.152= 10,92(g)
1/
Cu+ 2AgNO3 -----> Cu(NO3)2+ 2Ag
Khối lượng dd giảm: mdd↓=340*6%*25%=5.1
Ta luôn có mdd giảm=mKL tăng=5.1g
Khối lượng vật sau p/ư: mvật=15+5.1=20.1 g