cho mình hỏi:lưu huỳnh ở Wikipedia viết là chất rắn màu vàng chanh mà tại sao trong hóa học(trong chuương trình học) thì lưu huỳnh không phải là chất rắn mà ở thể lỏng hoặc thể khí vậy các bạn?(mình toàn thấy thí nghiệm tác dụng với lưu huỳnh có ai sử dụng chất rắn(đá lưu huỳnh) đâu.Mà lưu huỳnh còn cháy được nữa(nó là chất rắn tại sao lại thành chất khí và cháy được vậy?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Phương trình hóa học S + O2 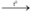 SO2
SO2
b) nS = 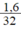 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 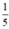 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l

a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
b. Số mol của S tham gia phản ứng:
nS = = 0,05 mol
Theo phương trình hóa học, ta có: = nS =
= 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 = 5 . 1,12 = 5,6 lít

a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia phản ứng :
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% về thể tích của không khí nên thể tích không khí cần dùng là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
Bạn Đặng Quỳnh Ngân có thể giải thích cho mk tại sao Vkk=5.VO2
mk chưa hiểu đoạn đó cảm ơn bạn

a) Phương trình phản ứng hóa học :
S + O2 →→ SO2
b) Số mol lưu huỳnh tham gia phản ứng :
nS=3,232=0,1(mol)nS=3,232=0,1(mol)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% về thể tích của không khí nên thể tích không khí cần dùng là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)

a/ PTHH: S + O2 =(nhiệt)==> SO2
b/ nS = 3,2 / 32 = 0,1 mol
=>nO2 = nSO2 = nS = 0,1 mol
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=>Vkhông khí = \(\frac{2,24.100}{20}\) = 11,2 lít

nFe = m/M= 16,8/56=0,3(mol)
nS = m/M= 6,4/32=0,2(mol)
PTHH: Fe + S = FeS
Trước phản ứng: 0,3 0,3 0,3 (mol)
Phản ứng: 0,3 0,2 (mol)
Sau phản ứng: 0 0,1 0,3 (mol)
a/ chất rấn A gồm Fe và S
b/ PTHH: FeS + 2HCl = Fecl2 + H2S
Theo phản ứng: 1 2 1 1 (mol)
Theo bài ra: 0,3 0,6 0,3 0,3 (mol)
vH2S = n.22,4=0,3.22,4=6,72(l)

(2) Lưu huỳnh có thể tác dụng với halogen như flo, clo
(5) Hidro sunfua là chất khí không màu, mùi trứng thối và rất độc
(7) Hidro sunfua có tính khử mạnh
ĐÁP ÁN C

a) PTHH: S + O2 =(nhiệt)=> SO2
b) nS = 3,2 / 32 = 0,1 (mol)
=> nO2 = nSO2 = nS = 0,1 (mol)
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VKK(đktc) = \(2,24\div\frac{1}{5}=11,2\left(l\right)\)



Lưu hình thể rắn ở điều kiện tự nhiên là đúng, người ta hay dùng những cụ vàng vàng để sấy tre lứa cho ko bị mốc ý. Còn lưu huỳnh dạng khí là lưu huỳnh đơn chất, được tách ra bởi pưhh, mà các phản ứng thường có nhiệt độ cao nên lưu huỳnh bay lên hòa vào lồng khí lưu thông hoặc chảy ra thành chất lỏng