1) cho một đinh sắt nặng 6 gam vào dung dịch CuSO4 1M có thể tích là 100 ml. Sau một thời gian lấy đinh sắt lau khô rồi đem cân lên thấy khối lượng là 6,12 gam.Tính C nồng độ mol của dung dịch sau phản ứng
2) đốt hoàn toàn 1.55g P thu đc chất a. Hòa tan a vào 200g h2o thu đc dung dịch b. Tính C% dd b?

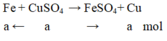
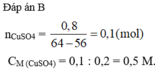
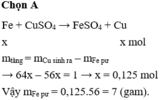
Bài 2:
nP = 0,05 mol
Pt: 4P + 5O2 --to--> 2P2O5
0,05 mol-----------> 0,025 mol
.....P2O5 + 3H2O --> 2H3PO4
0,025 mol----------> 0,05 mol
mH3PO4 = 0,05 . 98 = 4,9 (g)
mdd sau pứ = mP2O5 + mH2O = 0,025 . 142 + 200 = 203,55 (g)
C% dd H3PO4 = \(\dfrac{4,9}{203,55}.100\%=2,407\%\)
Bài 1:
Gọi a là số mol Fe pứ
nCuSO4 bđ = 1 . 0,1 = 0,1 mol
=> nCu = nCuSO4 = 0,1 mol
mtăng = 6,12 - 6 = 0,12g
Pt: Fe + CuSO4 --> FeSO4 + Cu
......a...........a................a...........a
Ta có: 64a - 56a = 0,12
=> a = 0,015 < 0,1 mol
=> CuSO4 không pứ hết
CM CuSO4 = (0,1 - 0,015)/0,1 = 0,85M
CM FeSO4 = 0,015/0,1 = 0,15M