cho 0.3 mol H2SO4 và 0.1 mol HCl vào 0.2 mol Ba(OH)2 và 0.3 mol NaOH thì quì tím sẽ chuyển sang màu gì
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) H 2 S O 4 + 2 N a O H → N a 2 S O 4 + 2 H 2 O
nNaOH = 2n H 2 S O 4 đúng theo phương trình. Sau phản ứng chỉ có H 2 S O 4 , nên môi trường trung tính không làm đổi màu quỳ tím.
HCl + KOH → KCl + H2O
nHCl > nKOH : HCl dư, quỳ tím chuyển màu đỏ.

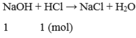
Sau phản ứng dung dịch thu được chỉ chứa NaCl, vậy dung dịch sau phản ứng không làm quỳ tím đổi màu.
Chọn đáp án C

Gọi CT chung của 2 axit là HX
______________ 2 bazơ là ROH
=> PTHH :
\(ROH+HX-->RX+H_2O\left(1\right)\)
0,4_____0,4__________0,4
\(n_{HX}=n_{HCl}+2n_{H_2SO_4}=0,1+0,2.2=0,5\left(mol\right)\)
\(n_{ROH}=n_{NaOH}+2n_{Ba\left(OH\right)_2}=0,2+0,1.2=0.4\left(mol\right)\)
=> HX dư => sau pứ quỳ chuyển sang đỏ

Đáp án B
X: CH3NH3NO3
mrắn = mNaOH dư + mmuối = 0,1. 40 + 0,1.85 = 12,5

a) mCuSO4 = n.M = 0,2 x 160 = 32 (gam)
b) VSO2(đktc) = n.22,4 = 0,45 x 22,4 = 10,08 (lít)
c)???
d) mAl(OH)3 = n.M = 0,3 x 78 = 23,4 gam
e) VSO2(đktc) = n.22,4 = 0,45 x 22,4 = 10,08 lít