đốt cháy hoàn toàn m g chất A dùng hết 5.824 l O2 sản phẨM CO2 , H2O đc chia đôi. phần 1 cho đi qua P2O5 thấy lượng P205 tăng thêm 1.8 g , phần 2 cho đi qua CaO thấy lượng CaO tăng 5.32 g tìm m và CTPT A và cho bt A ở thể khí (đk thường) có số cacbon bé hơn hoặc bằng 4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


+ Lọ P2O5 bắt H2O -> mH2O = 1,8(gam) -> nH2O = 0,1(mol)
+ Lọ 2 bắt H2O và CO2: mCO2 = 5,32 -1,8 = 3,52(gam) -> nCO2 = 0,08(mol)
nCO2 = \(\frac{5,824}{22,4}\) = 0,26(mol)
Theo định luật bảo toàn khối lượng:
m + mO2 = mCO2 + mH2O
m = 2.5,32-0,26.32= 2,32(gam)
nC = nCO2 = 2.0,08 = 0,16(mol)
-> mC = 1,92(gam)
nH = 2nH2O = 2.2.0,1 = 0,4(mol)
-> mH = 0,4(gam)
mO = 2,32 - 1,92 - 0,4 = 0
X chỉ gồm C và H.
nC: nH = 0,16 : 0,4 = \(\frac{2}{5}\)
CTPT là (C2H5)n
Ta có: \(2n\le4->n\le2\)
Có 2 nghiệm n = 1 (C2H5) -> loại
n = 2 (C4H10) -> chọn

- Bình P2O5 bắt H2O \(\rightarrow\)\(m_{H_2O}=1,8g\rightarrow n_{H_2O}=0,1mol\)
- Bình 2 bắt H2O và CO2:\(m_{CO_2}=5,32-1,8g=3,52g\rightarrow n_{CO_2}=0,08mol\)
\(n_{O_2}=\dfrac{5,824}{22,4}=0,26mol\)
- Áp dụng định ;uật BTKL:
\(m+m_{O_2}=m_{CO_2}+m_{H_2O}\)
m=2.5,32-0,26.32=2,32g
\(n_C=n_{CO_2}=2.0,08=0,16mol\rightarrow m_C=1,92g\)
\(n_H=2n_{H_2O}=2.2.0,1=0,4mol\rightarrow m_H=0,4g\)
\(m_O=2,32-1,92-0,4=0\)
Nghĩa là A chỉ gồm C và H.
\(n_C:n_H=0,16:0,4=2:5\)
- Công thức đơn giản nhất của A là C2H5
- Công thức thực nghiệm: \(\left(C_2H_5\right)_n\)
- Ta có: 2n\(\le\)4\(\rightarrow\)n\(\le\)2 có 2 nghiệm n=1( C2H5 loại) và n=2( C4H10 chọn)

Đáp án B.
n C O 2 = 1 m o l ; Bình 1 chỉ giữ H2O ở lại mà polietilen
n C O 2 = n H 2 O ⇒ m H 2 O = 1 : 18 = 18 gam

Khi A tác dụng với O 2 chỉ sinh ra, và H 2 O , vậy A có chứa cacbon, hiđro, có thể có hoặc không có oxi.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m A + m O 2 = 7,30 (g) (1)
Theo đầu bài: m C O 2 + m H 2 O = 3,70(g). (2)
Từ hệ (1) và (2), tìm được m C O 2 = 5,50 g; m H 2 O = 1,80 g.
Khối lượng C trong 5,50 g
C
O
2
: 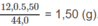
Khối lượng H trong 1,8 g
H
2
: 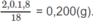
Đó cũng là khối lượng c và H trong 2,50 g chất A. Vậy chất A phải chứa O.
Khối lượng O trong 2,50 g A: 2,50 - 1,50 - 0,200 = 0,80 (g)
Phần trăm khối lượng của C: 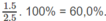
Phần trăm khối lương của H: 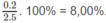
Phần trăm khối lương của O: 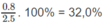

\(\text{nO2 56/22,4 = 2,5 mol}\)
Phần 1: m bình tăng = mH2O = 9 (g) => nH2O = 9/18 = 0,5 mol
Phần 2: m bình tăng = mCaO + mH2O
\(\text{=> mCO2 = 53 - 0,5.18 = 44 (g) => nCO2 = 1 mol}\)
Như vậy đốt toàn bộ a gam A thì thu được 1 mol H2O và 2 mol CO2 (nhân đôi số liệu do chia làm 2p bằng nhau)
BTKL: mA + mO2 = mCO2 + mH2O \(\text{=> a + 2,5.32 = 2.44 + 1.18 => a = 26 (g)}\)
BTNT "C" => nC(A) = nCO2 = 2 mol
BTNT "H" => nH(A) = 2nH2O = 2 mol
BTKL: mO(A) = 26 - 2.12 - 2.1 = 0 (g) => A không chứa O
Tỉ lệ C : H = 2 : 2 = 1 : 1
=> CTĐGN là CH
Do A có số C <= 2 => CTPT là C2H2

Đáp án C
nX =0,4 mol
Khối lượng bình 1 đựng P2O5 tăng là số lượng của H2O.
Khối lượng bình đựng KOH rắn tăng chính là khối lượng của CO2
Khi đốt cháy 1 anken ta luôn có: ![]()
![]()
![]()
![]() anken là C3H6 và C4H8
anken là C3H6 và C4H8
Gọi phần trăm thể tích về thể tích của C3H6 là x% thì phần trăm thể tích về thể tích của C4H8 là
(100 -x) %
Ta có:
![]()
![]()

\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} = \dfrac{3}{100} = 0,03(mol)\\ n_{H_2O} = \dfrac{2,04-0,03.44}{18} = 0,04(mol)\)
Vì \(n_{H_2O} > n_{CO_2}\) nên CTHH của X: CnH2n+2
\(n_X = n_{H_2O} - n_{CO_2} = 0,01(mol)\\ n = \dfrac{n_{CO_2}}{n_X} = \dfrac{0,03}{0,01} = 3\)
Vậy X là C3H8
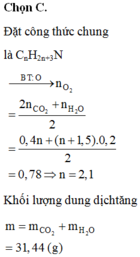
nO2 = 0.26 (mol)
P2O5 hút H2O => 1/2nH2O = 0.1 (mol) => nH2O = 0.2 (mol)
CaO hút cả H2O lẫn CO2 => 1/2mH2O + 1/2mCO2 = 5.32 (g)
<=> 0.1x18 + 1/2mCO2 = 5.32 => mCO2 = 7.04 (g) => nCO2 = 0.16 (mol)
CxHyOz + (x+y/2-z/4)O2 --to--> xCO2 + y/2H2O
___a___ax+0.5ay-0.25az_______ax____0.5ay_
Có ax+0.5ay-0.25az = 0.26
Có ax = 0.16
Có 0.5ay = 0.2 => ay = 0.4
=> az = 0.4
Vậy x : y : z = ax : ay : az = 0.16 : 0.4 : 0.4 = 2 : 5 : 5