ĐỀ 1
Câu 1: Thế nào là phản ứng hóa hợp? Cho ví dụ.
Câu 2: Bổ túc và hoàn thành các phương trình sau:
a. K + O2
b. C2H2 + O2
c. P + O2
d. Al + O2
d. C + O2
e. Fe + O2
Câu 3: Cho Fe2O3 , HCl , SiO2 , N2O5 , Na2SO4 , CuO. Xác định oxit axit , oxit bazơ và đọc tên
Câu 4: Nêu hiện tượng và viết phương trình hóa học khi đốt cháy sắt trong oxi.
Câu 5: Đốt cháy phốt pho đỏ trong bình đựng khí oxi, sau phản ứng thu được 42,6g điphotpho pentaoxit
a. Viết phương trinh phản ứng
b. Tính khối lượng photpho tham gia phản ứng
c. Tính thể tích khí oxi đã dùng (đktc)
ĐỀ 2
Câu 1: Thế nào là oxit ? Cho ví dụ.
Câu 2: Cân bằng phương trình và cho biết phản ứng nào là phản ứng hóa hợp?
a. Fe(OH)3 -> Fe2O3 + H2O
b. Al + S -> Al2S3
c. MgCl2 + NaOH -> Mg(OH)2 + NaCl
d. K2O + P2O5 -> K3PO4
e. Na + H2O -> NaOH + H2
Câu 3: Cho P2O5 , MgO , CaCO3 , K2O , SO2 , KNO3. Xác định oxit axit , oxit bazơ và đọc tên
Câu 4: Nêu hiện tượng và viết phương trình hóa học khi đốt cháy lưu huỳnh trong oxi.
Câu 5: Đốt cháy 6,72 lit khí metan trong bình đựng khí oxi
a. Viết phương trinh phản ứng
b. Tính khối lượng sản phẩm
c. Tính thể tích khí oxi đã dùng (đktc)
ĐỀ 3
Câu 1: Thế nào là sự oxi hóa ? Cho ví dụ
Câu 2: Cân bằng phương trình và cho biết phản ứng nào là phản ứng hóa hợp?
a. P2O5 + H2O -> H3PO4
b. C3H6 + O2 -> CO2 + H2O
c. Al + HCl -> AlCl3 + H2
d. Na + O2 -> Na2O
e. KMnO4 -> K2MnO4 + MnO2 + O2
Câu 3: Cho SO3 , KOH , Na2O , CO2 , CaO , H2SO4. Xác định oxit axit , oxit bazơ và đọc tên
Câu 4: Nêu hiện tượng và viết phương trình hóa học khi đốt cháy photpho trong oxi.
Câu 5: Đốt cháy lưu huỳnh trong bình đựng khí oxi thu được 24g khí lưu huỳnh đioxit
a. Viết phương trinh phản ứng
b. Tính khối lượng lưu huỳnh tham gia phản ứng.
c. Tính thể tích khí oxi đã dùng (đktc)
ĐỀ 4
Câu 1: Thế nào là oxit ? Cho ví dụ
Câu 2: Cân bằng phương trình và cho biết phản ứng nào là phản ứng hóa hợp?
a. H2 + O2 -> H2O
b. CaCO3 -> CaO + CO2
c. SO2 + O2 -> SO3
d. KClO3 -> KCl + O2
e. C2H4 + O2 -> CO2 + H2O
Câu 3: Cho Fe3O4 , BaO , ZnCl2 , NO2 , KMnO4 , HgO. Xác định oxit axit , oxit bazơ và đọc tên
Câu 4: Hãy chỉ ra công thức sai và sửa lại cho đúng: KSO4, Al(OH)3, MgCl, CaO, ZnO , HCl .
Câu 6: Đốt cháy 33,6g sắt trong bình đựng khí oxi, sau phản ứng thu được oxit sắt từ
a. Viết phương trinh phản ứng
b. Tính thể tích khí oxi đã dùng (đktc)
c. Tính khối lượng sản phẩm.
ĐỀ 5
Câu 1: Có mấy loại oxit, nêu định nghĩa ? Cho ví dụ
Câu 2: Bổ túc và hoàn thành các phương trình sau:
a. Mg + O2 ->
b. C3H8 + O2 ->
c. S + O2 ->
d. Cu + O2 ->
d. P + O2 ->
e. Fe + O2 ->
Câu 3: Cho FeO , Cu(OH)2 , Ag2O , KClO3 , P2O3 , PbO. Xác định oxit axit , oxit bazơ và đọc tên
Câu 4: Nhận biết 2 lọ đựng khí mất nhãn sau: khí oxi và khí cacbonnic
Câu 5: Đốt cháy 10,8g nhôm trong bình đựng khí oxi, sau phản ứng thu được nhôm oxit
a. Viết phương trinh phản ứng
b. Tính khối lượng sản phẩm
c. Tính thể tích không khí biết thể tich khi oxi chiếm 20% thể tích không khi.
ĐỀ 6
Câu 1: Nêu tính chất hóa học của oxi ? Cho ví dụ
Câu 2: Bổ túc và hoàn thành các phương trình sau:
a. Zn + O2 ->
b. C4H10 + O2 ->
c. Ba + O2 ->
d. Na + O2 ->
d. C + O2 ->
e. Ca + O2 ->
Câu 3: Cho Ca(OH)2 , K2O , Al2O3 , HNO3 , SiO2 , PbO. Xác định oxit axit , oxit bazơ và đọc tên
Câu 4: Nhận biết 2 lọ đựng khí mất nhãn sau: khí nitơ và khí cacbonnic
Câu 5: Đốt cháy 7,2g magie trong bình đựng khí oxi, sau phản ứng thu được magie oxit
a. Viết phương trinh phản ứng
b. Tính khối lượng sản phẩm
c. Tính thể tích không khí biết thể tich khi oxi chiếm 20% thể tích không khi.
MÌNH CẦN GẤP MONG CÁC BẠN GIÚP ĐỠ, CẢM ƠN CÁC BẠN



![]()
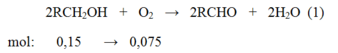
![]()
![]()
Oxi lỏng (1877)
Năm 1877, L.-P. Cailletet (1832-1913), chủ một xưởng thợ rèn của Côte-d’Or (Bourgogne) đã phát minh ra một chiếc bơm cho phép tạo ra và duy trì được áp suất cỡ vài trăm atmotphe.
Ông đã hóa lỏng được oxi bằng cách gây ra sự giãn nở đột ngột của chất khí chứa trong một mao quản mà ở đó ông đã giảm áp suất từ 300 tới 1 atmotphe, điều đó khiến cho nhiệt độ hạ xuống tới -118,9oC.
Vài ngày sau khi thí nghiệm thành công đó, R.-P. Pictet (1848-1929), giáo sư vạt lý ở Đại học Giơnevơ đã công bố kết quả của các nghiên cứu tương tự.
Không khí lỏng (1895)
Năm 1895, nhà phát minh và nhà công nghiệp K. von Linde (1842-1934) đã hóa lỏng được không khí bằng cách nén và cho giãn nở với sự làm lạnh trung gian. Như vậy là ông đã điều chế được oxi lỏng gần như tinh khiết. năm 1902, nhà bác học G. Claude (1870-1960) đã phát minh ra một phương pháp khác để hóa lỏng không khí, bằng cách cho giãn nở chất khí với việc sản công bên ngoài. Xuất phát tự không khí khóa lỏng, ông đã tách được oxi, nitơ và agon lỏng bằng cách phân đoạn. Như vậy, ông đã tìm ra phương pháp công nghiệp đầu tiên để hóa lỏng chất khí.