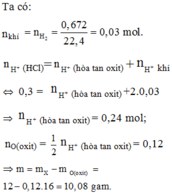Cho m Fe phản ứng với oxi sau một thời gian thu được 4,64g hỗn hợp các oxit FeO,Fe2O3,và Fe3O4. Cho hỗn hợp oxit tác dụng hòa tan với dd HCl 1M thì cần vừa đủ 160ml . Xác định giá trị m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a) 4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3\\ 2Fe + O_2 \xrightarrow{t^o}2FeO\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\)
b)
Bảo toàn khối lượng :
\(m_{kim\ loại} + m_{O_2} = m_{oxit}\\ \Rightarrow n_{O_2} = \dfrac{19,2-14,8}{32} = 0,1375(mol)\\ V_{O_2} = 0,1375.22,4 =3,08(lít)\)
c)
\(n_{O(oxit)} = 2n_{O_2} = 0,1375.2 = 0,275(mol)\\ 2H^+ + O^{2-} \to H_2O\\ n_{HCl} = n_{H^+} = 2n_O = 0,275.2 = 0,55(mol)\\ m = 0,55.36,5 = 20,075(gam)\)

\(\left\{{}\begin{matrix}n_{HCl}=0,2.4=0,8\left(mol\right)\\n_{HBr}=0,2.2=0,4\left(mol\right)\end{matrix}\right.\)
=> \(n_{H_2O}=0,6\left(mol\right)\)
=> nO = 0,6 (mol)
=> mkim loại = 34,8 - 0,6.16 = 25,2 (g)
=> mmuối = 25,2 + 0,8.35,5 + 0,4.80 = 85,6 (g)


Chào bạn tuy không thể giúp bạn nhưng cho mình hỏi bạn có bị mất thanh thông báo tin nhắn như mình không ạ

Tương tự bài 1 và bài 4, ta có:
m 3 o x i t + m H C l = m m u o i + m H 2 O s a n p h a m
⇔ m 3 o x i t = m m u o i + m H 2 O s a n p h a m - m H C l
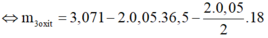
⇔ m 3 o x i t = 0,321g
⇒ Chọn D.

Mình làm câu này rồi nè, bạn tham khảo bài làm của mình ở link này nha
https://hoc24.vn/cau-hoi/hoa-tan-hoan-toan-576-gam-hon-hop-a-gom-fe3o4-fe2o3-feo-fe-trong-dung-dich-hcl-thi-can-dung-360-gam-dung-dich-hcl-1825-de-tac-dung-vua-du-sau-phan-ung-thu-duoc-v-lit-h2-dktc-va-dung-dich-b-c.1336663119282

a) \(n_{HCl}=\dfrac{360.18,25\%}{36,5}=1,8\left(mol\right)\)
Sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam.
\(n_{H_2}=n_{O\left(trongCuO\right)}=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H: \(n_{HCl}=2n_{H_2}+2n_{H_2O}\Rightarrow n_{H_2O}=0,7\left(mol\right)\)
=> \(n_{O\left(trongA\right)}=0,7\left(mol\right)\)
\(m_{muối}=m_{Fe}+m_{Cl}=\left(57,6-0,7.16\right)+1,8.35,5=110,3\left(g\right)\)
b) B gồm FeCl3 và FeCl2
Gọi x,y lần lượt là số mol của FeCl2 và FeCl3
\(\left\{{}\begin{matrix}3x+2y=1,8\\162,5x+127y=110,3\end{matrix}\right.\)
=> \(x=\dfrac{1}{7};y=\dfrac{24}{35}\)
\(m_{ddB}=m_A+m_{ddHCl}-m_{H_2}=417,2\left(g\right)\)
=> \(C\%_{FeCl_3}=\dfrac{\dfrac{1}{7}.162,5}{417,2}.100=5,56\%\)
\(C\%_{FeCl_2}=\dfrac{\dfrac{24}{35}.127}{417,2}.100=20,87\%\)
c) \(n_{HCl\left(bđ\right)}=2.2=4\left(mol\right)\)
Nếu trong X chỉ chứa Fe3O4 thì :
\(n_{HCl}=8n_{Fe_3O_4}=8.\dfrac{100}{232}=3,45\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe2O3 thì :
\(n_{HCl}=6n_{Fe_3O_4}=6.\dfrac{100}{160}=3,75\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa FeO thì :
\(n_{HCl}=2n_{FeO}=2.\dfrac{100}{72}=2,78\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe thì :
\(n_{HCl}=2n_{Fe}=2.\dfrac{100}{56}=3,57\left(mol\right)< n_{HCl\left(bđ\right)}\)
=> HCl luôn dư và X luôn tan hết