Một oxit sắt có thành phầm về khối lượng là mFe: mO = 7:3. Hỏi màu của oxit trên là màu gì?
A. Xanh
B. Đen
C. Trắng
D. Nâu đỏ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. Gọi CTHH của oxit là NxOy.
Ta có: \(\dfrac{m_N}{m_O}=\dfrac{7}{20}\Rightarrow\dfrac{n_N}{n_O}=\dfrac{7}{20}:\dfrac{14}{16}=\dfrac{2}{5}\)
⇒ x:y = 2:5
→ N2O5
2. Gọi CTHH cần tìm là FexOy.
\(\Rightarrow\dfrac{m_{Fe}}{m_O}=\dfrac{7}{2}\Rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{7}{2}:\dfrac{56}{16}=1\)
⇒ x:y = 1
→ FeO
3. CTHH cần tìm: RO2
Mà: %R = 46,7%
\(\Rightarrow\dfrac{M_R}{M_R+16.2}.100\%=46,7\%\)
⇒ MR = 28 (g/mol)
→ SiO2

Đồng oxit nào mà có M= 20(g/mol) được em.
Nhưng em bảo 80% Cu, 20% O thì anh thấy chắc là CuO rồi nè
sửa đề M = 80 g/mol
\(n_{Cu}=\dfrac{80.80\%}{64}=1\left(mol\right)\\ n_{O_2}=\dfrac{80-64}{16}=1\left(mol\right)\\ Cthh:CuO\)

a) Gọi CTHH của oxit sắt là FexOy ( x,y \(\in\) N* )
Theo đề , ta có: %mO = \(\frac{m_O}{m_{hc}}.100\%\)
=> 30% = \(\frac{16x}{56x+16y}.100\%\)
=> 0,3( 56x + 16y ) = 16y
=> 16,8x + 4,8y = 16y
=> 16,8x = 11,2y
=> \(\frac{x}{y}=\frac{11,2}{16,8}=\frac{2}{3}\)
Vậy CTHH cần tìm của oxit là Fe2O3
b) Gọi x,y lần lượt là số mol của Fe,O ( x,y > 0 )
Theo đề, ta có: \(\frac{m_{Fe}}{m_O}=\frac{7}{3}\)
=> \(\frac{56x}{16y}=\frac{7}{3}\)
=> 56x.3 = 16y.7
=> 168x = 112y
=> \(\frac{x}{y}=\frac{2}{3}\)

b)
%Ca : %C : %O = 10 :3 : 12
=> 40.nCa : 12.nC : 16.nO = 10 : 3 : 12
=> nCa : nC : nO = 1 : 1 : 3
=> CTHH: CaCO3
c)
24.nMg : 12.nC : 16.nO = 2:1:4
=> nMg : nC : nO = 1 : 1 : 3
=> CTHH: MgCO3
\(n_{MgCO_3}=\dfrac{8,4}{84}=0,1\left(mol\right)\)
=> Số nguyên tử Mg = 0,1.1.6.1023 = 0,6.1023
=> Số nguyên tử C = 0,1.1.6.1023 = 0,6.1023
=> Số nguyên tử O = 0,1.3.6.1023 = 1,8.1023
a: Theo đề, ta có:
\(\dfrac{n_{Fe}\cdot56}{n_O\cdot16}=\dfrac{21}{8}\Leftrightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{3}{4}\)
Vậy: Công thức là \(Fe_3O_4\)

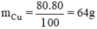
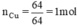 nguyên tử Cu.
nguyên tử Cu.
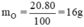
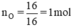 nguyên tử O.
nguyên tử O.
Suy ra trong 1 phân tử hợp chất có 1 nguyên tử Cu và 1 nguyên tử O.
Do đó công thức của oxit đồng màu đen là CuO.
Gọi CTHH của oxit sắt là $Fe_xO_y$
Ta có :
$\dfrac{56x}{16y} = \dfrac{7}{3} \Rightarrow \dfrac{x}{y} = \dfrac{7}{3} : \dfrac{56}{16} = \dfrac{2}{3}$
Vậy oxit là $Fe_2O_3$(màu nâu đỏ)
\(CT:Fe_xO_y\)
\(56x:16y=7:3\)
\(\Rightarrow x:y=2:3\)
\(CT:Fe_2O_3\)
=> nâu đỏ