Khử hoàn toàn 6 g X gồm Fe, FeO, Fe2O3, Fe3O4 bằng H2 dư thu được 5,04 g Fe. Tính thể tích SO2 ở đktc thoát ra khi hòa tan X trong H2SO4 đặc, nóng, dư.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{Fe}=\dfrac{12,6}{56}=0,225\left(mol\right)\)
Coi X gồm Fe và O.
BTNT Fe: nFe (X) = 0,225 (mol)
Ta có: \(n_{SO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
BT e, có: 3nFe = 2nO + 2nSO2 ⇒ nO = 0,2625 (mol)
⇒ m = mFe + mO = 0,225.56 + 0,2625.16 = 16,8 (g)

Đáp án C
Tương tự Câu 8, áp dụng công thức giải nhanh ta có:
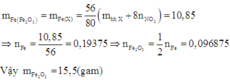

Đáp án A
Quy đổi hỗn hợp thành Fe và O với số mol là x và y → 56x + 16y =17,04 g
nNO =0,015 mol → nH+(A)=0,06 mol
Bảo toàn số mol H+ có nHCl = 2nH2 +2nO + nH+(A) → nO= y=(0,66 -0,06-2.0,075):2=0,225 mol
→ x =0,24 mol
Khi cho AgNO3 vào dd A thì tạo ↓ AgCl và Ag
Bảo toàn số mol Cl thì AgCl : 0,66 mol
Bảo toàn e cho toàn bộ quá trình thì 3x =2.0,075 + 2.0,225 +3.0,015+ nAg→ nAg=0,075 mol
→ m =0,075.108 +0,66 .143,5=102,81 g

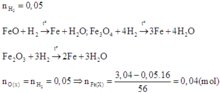
Coi hỗn hợp X ban đầu gồm Fe và O.
Khi đó áp dụng định luật bảo toàn mol electron, ta có:
![]()
Đáp án A.

Đáp án A
Quy hỗn hợp X về dạng Fe và O.
=> mX = 56nFe + 16nO = 14,4g (1)
- Khi X + H2SO4: Bảo toàn e: 3nFe = 2nO + 2nSO2
=> 3nFe – 2nO = 2.6,72: 22,4 = 0,6 mol (2)
Từ (1,2) => nFe = 0,24; nO = 0,06 mol
Vậy muối trong dung dịch sau phản ứng sẽ là: 0,12 mol Fe2(SO4)3
=> mFe2(SO4)3 = 0,12.400 = 48g

Đáp án : B
Nếu NaOH dư => n F e O H 3 = 0,2 mol
=> nFe(bd) = 0,2 mol
=> nO(bd) = 0,5 mol. Vô lý
(Vì số mol O trong oxit cao nhất là gấp 1,5 lần số mol Fe).
Vậy NaOH thiếu : 19,2 F e : a O : b
56a + 16b = 19,2
n H 2 S O 4 = 0 , 9
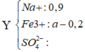
→ B T D T n S O 4 2 - = 0 , 3 + 3 a 2
→ B T N T . S n S O 2 = 0 , 9 - 0 , 3 + 3 a 2 a
6a – 2b = 1,5 ⇒ a = 0 , 3 b = 0 , 15 → V = 6 , 72

Đáp án : A
Do H2SO4 đặc dư => phản ứng tạo Fe3+
=> nkết tủa = nFe(OH)3 = 0,2 mol
Mà nNaOH = 0,9 mol > 3nFe(OH)3 => nOH trung hoà = 0,9 – 3.0,2 = 0,3 mol
=> nH2SO4 phản ứng X = 0,75 mol
Coi X gồm x mol Fe và y mol O
=> nH+ = 6nFe - 2nO = > 1,5 = 6x – 2y
, mX= 56x + 16y =19,2g
=> x = 0,3 mol ; y = 0,15 mol
=> BT e : nSO2.2 + nO.2= 3nFe => nSO2 = 0,3 mol
=> VSO2 = 6,72 lit
