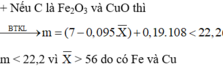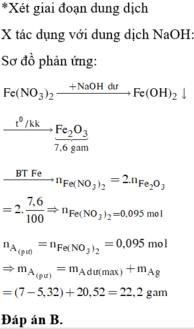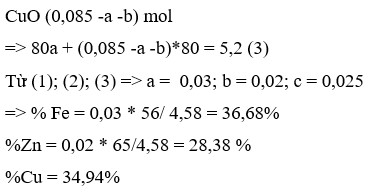Cho dung dịch NaOH 0,5M dư vào 7,2g hổn hợp Fe2(SO4)3 va CuSO4. Lọc kết tủa rửa nhẹ, đem nung đến khối lượng không đổi được 3,2g chất rắn. Tính % khối lượng mỗi muối, tính V NaOH
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CuSO4+2NaOH---->Cu(OH)2+Na2SO4
Al2(SO4)3+6NaOH----> 2Al(OH)3+3Na2SO4
Al(OH)3+NaOH--->NaAlO2+2H2O
Cu(OH)2--->CuO+H2O
n CuSO4=0,1.1=0,1(mol)
n Al2(SO4)3=0,1.1=0,1(mol)
Do NaOH dư nên Al(OH)3 bị hòa tan. Chất rắn sau khi nung chỉ còn CuO
Theo pthh1
n\(_{Cu\left(OH\right)2}=n_{CuSO4}=0,1\left(mol\right)\)
Theo pthh4
n\(_{CuO}=n_{CuSO4}=0,1\left(mol\right)\)
m\(_{CuO}=0,1.80=8\left(g\right)\)
\(\text{nCuSO4 = 0,1 mol; nAl2(SO4)3 = 0,1 mol}\)
Al2(SO4)3 + 6NaOH -> 2Al(OH)3 + 3Na2SO4
Al(OH)3 + NaOH dư -> NaAlO2 + 2H2O
CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
(mol)...0,1...............................-> 0,1
Kết tủa thu được chỉ có Cu(OH)2
Nung kết tủa: Cu(OH)2 ->..CuO + H2O
(mol)................0,1....................-> 0,1
\(\text{Khối lượng chất rắn = mCuO = 0,1. 80 = 8 gam }\)

PTHH: CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2 ↓
Số mol của CuSO4 là: 16 : 160 = 0,1 mol
So sánh : 0,1 < \({0,3\over 2}\)
=> NaOH dư. Tính theo CuSO4
Số mol của Cu(OH)2 kết tủa là: 0,1 mol
Khôiư lượng chất kết tủa là: 0,1 . 98 = 9,8 gam