Có 2 kim loại A và B. Cho dòng khí CO dư đi qua ống sứ nung nóng chứa hỗn hợp X gồm 2 oxit của 2 kim loại trên đến khi phản ứng hoàn toàn thì còn lại chất rắn Y trong ống và khí Z đi ra khỏi ống. Dẫn khí Z vào cốc đựng lượng dư dd Ba(OH)2 thu đc 2,955g kết tủa. Cho Y tác dụng với dd H2SO4 10% vừa đủ thì ko có khí thoát ra, còn lại 0,96g chất rắn không tan và tạo ra dung dịch T có nồng độ...
Đọc tiếp
Có 2 kim loại A và B. Cho dòng khí CO dư đi qua ống sứ nung nóng chứa hỗn hợp X gồm 2 oxit của 2 kim loại trên đến khi phản ứng hoàn toàn thì còn lại chất rắn Y trong ống và khí Z đi ra khỏi ống. Dẫn khí Z vào cốc đựng lượng dư dd Ba(OH)2 thu đc 2,955g kết tủa. Cho Y tác dụng với dd H2SO4 10% vừa đủ thì ko có khí thoát ra, còn lại 0,96g chất rắn không tan và tạo ra dung dịch T có nồng độ 11,243%.
a, Xác định A,B và công thức của các oxit đã dùng.
b, Xác định % theo khối lượng của mỗi chất trong hỗn hợp X, biết rằng khi hoà tan hết X vào dd HCl thì nồng độ % của 2 muối trong dd là như nhau.




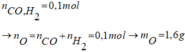

(a) Vì khi cho chất rắn thu được sau phản ứng với CO tác dụng với dung dịch HCl tạo ra khí H2 nên R phải là kim loại đứng sau Al và đứng trước hidro trong dãy hoạt động hóa học. Đặt công thức oxit của R là RxOy.
CuO + CO → Cu + CO2
a a
RxOy + yCO → xR + y CO2
c xc
Al2O3 + 6HCl → RCln + n/2 H2
xc nxc xc nxc/2
Đạt các mol CuO, Al2O3, RxOy trong 6,1 g hỗn hợp A là a,b,c. Có
80a + 102b+ (xMr + 16y)c = 6,1
1,28 + 102b + Mrxc = 4,82
64a = 1,28
6b + nxc = 0,15
nxc/2 = 0,045
=> a = 0,02
=> nxc = 0,09
b = -0,01
Mr = 28n
=> n = 2 , Mr = 56, R là Fe
xc = 0,45 => yc = 0,06
x/y = 0,045/0,06 = 3/4
=> x = 3, y = 4 CT oxit = Fe2O3
bạn ơi bài trên giải sai thì phải
sao al2o3+có lại được rcln+h2