hòa tan 25,8 gam hh gồm bột Al và Al2O3 trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí Hiđro. Khối lượng muối AlCl2 thu được là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Cho phần 1 tác dụng với 0,4 mol NaOH thấy thoát ra 0,04 mol H2.
Do vậy Al dư 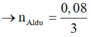
BTNT: ![]()
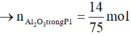
Ta có khối lượng mỗi phần là 39,44 gam.
![]()
Phần 2 tan trong HCl thu được dung dịch Z chứa 98,64 gam muối.
![]()
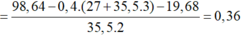
Giải được số mol Cr và Fe trong mỗi phần là 0,12 và 0,24 mol.
Bảo toàn O:
![]()
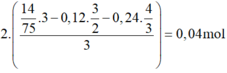

Đáp án A
Cho phần 1 tác dụng với 0,4 mol NaOH thấy thoát ra 0,04 mol H2.
Do vậy Al dư
→ n A l d ư = 0 , 08 3 B T N T : n A l ( P 1 ) = n N a O H = 0 , 4 → n A l 2 O 3 t r o n g P 1 = 14 75 m o l
Ta có khối lượng mỗi phần là 39,44 gam.
→ m C r + m F e = 19 , 68 g a m
Phần 2 tan trong HCl thu được dung dịch Z chứa 98,64 gam muối.
→ n C r + n F e = 98 , 64 - 0 , 4 ( 27 + 35 , 5 . 3 ) - 19 , 68 35 , 5 . 2 = 0 . 36
Giải được số mol Cr và Fe trong mỗi phần là 0,12 và 0,24 mol.
Bảo toàn O:
n A l 2 O 3 t r o n g X = 2 14 75 . 3 - 0 , 12 . 3 2 - 0 , 24 . 4 3 3 = 0 , 04 m o l → % A l 2 O 3 = 5 , 17 %







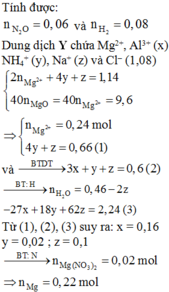
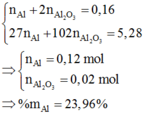
Al2O3+6HCl=>2AlCl3+3H2O (1)
2Al+6HCl=>2AlCl3+3H2 (2)
nH2=0,6:2=0,3mol
=> nAl=0,2mol=>mAl=27.0,2=5,4g=>mAl2O3=25,8-5,4=20,4g
=> nAl2O3=0,2mol
=> nAl2Cl3 (1)=2nAl2O3=0,2.2=0,4mol
nAlCl2(2)=nAl=0,2mol
=> m AlCl3=(0,4+0,2).133,5=80,1g
chỗ cuối là AlCl2 nha chứ k phải 3 mik ghi nhầm