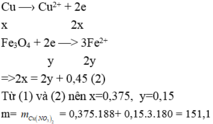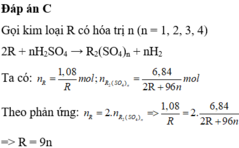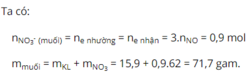cho 1,08g kim loại M vào dd \(H_{_{ }2}SO_{_{ }4}\) loãng dư. Lọc dd đem cô cạn thu được 6,84g 1 muối khan duy nhất. Vậy kim loại M là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



2 Z + n H 2 S O 4 → Z 2 S O 4 n + n H 2
Ta có:
m Z + m S O 4 2 - = m m u o i
m S O 4 2 - = m m u o i - m Z
= 6,84-1,08=5,76g
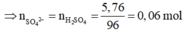
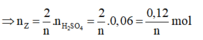
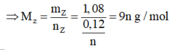
Thử chọn lần lượt n=1, 2, 3 ta được Z là kim loại Al hóa trị III
⇒ Chọn C.

Đặt hóa trị R là \(n(n\in \mathbb{N^*})\)
\(2R+nH_2SO_4\to R_2(SO_4)_n+nH_2\\ \Rightarrow n_R=2n_{R_2(SO_4)_n}\\ \Rightarrow \dfrac{2,16}{M_R}=\dfrac{27,36}{2M_R+96n}\\ \Rightarrow 27,36M_R=4,32M_R+207,36n\\ \Rightarrow M_R=9n\)
Thay \(n=3\Rightarrow M_R=27(g/mol)\)
Vậy R là nhôm (Al)

n(AgNO3) = 1.0,2 = 0,2mol
2AgNO3 + M → M(NO3)2 + 2Ag
0,2 0,1 m
[M(NO3)2] = 0,1(M+124) = 18,8g
→ M = 64. M là Cu
=> Đáp án D

Đáp án A
Gọi x, y lần lượt là số mol Cu va Fe3O4 phản ứng
=>64x + 232y = 61,2 – 2,4 = 58,8 (1)
Sau phản ứng còn 2,4 gam kim loại đó là Cu, nên trong dung dịch có Cu2+, Fe2+