Chia 10 gam hỗn hợp gồm 2 kim loại A,B có hoá trị không đổi thành 2 phần bằng nhau. Phần 1 đốt cháy hoàn toàn cần V lít khí O2 ở đktc, thu được 5,32 gam hỗn hợp 2 oxit. Phần còn lại hoà tan hoàn toàn trong dung dịch hcl (dư) thấy có V' lít khí H2 thoát ra ở đktc và m gam muối clorua. Tính các giá trị: V, V', m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Vì hai kim loại X, Y đều có hóa trị không đổi và khối lượng hai phần bằng nhau nên ở hai phần, số mol electron mà kim loại nhường bằng nhau.
Khi đó
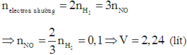

Chọn đáp án B
phản ứng trung hòa: –COOH + NaOH → –COONa + H2O
||→ có 0,02 mol NaOH → nCOOH = 0,02 mol → nO trong axit béo = 0,04 mol
(vì toàn bộ Oxi trong axit đều nằm trong nhóm COOH).
Đốt hỗn hợp axit + O2 → 0,35 mol CO2 + 0,34 mol H2O.
||→ bảo toàn O có nO2 = (0,35 × 2 + 0,34 – 0,04) ÷ 2 = 0,5 mol
||→ VO2 = 11,20 lít

\(n_{H_2}=\dfrac{0,953m}{22,4}=0,042545m\left(mol\right)\\ Đặt:n_{Mg}=x\left(mol\right);n_{Al}=y\left(mol\right);n_{Cu}=z\left(mol\right)\left(x,y,z>0\right)\\\Rightarrow \left\{{}\begin{matrix}24x+27y+64z=m\\40x+51y+80z=1,72m\\x+1,5y=0,042545m\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}x\approx0,012845m\\y\approx0,0198m\\z\approx0,002455m\end{matrix}\right.\\ \Rightarrow\%m_{Cu}\approx\dfrac{0,002455.64m}{m}.100\%\approx15,712\%\\ \%m_{Al}\approx\dfrac{27.0,0198m}{m}.100\%\approx53,46\%\\ \%m_{Mg}\approx\dfrac{0,012845.24m}{m}.100\%\approx30,828\%\)

Chọn D
Áp dụng bảo toàn khối lượng:
![]()
![]()

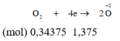
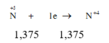
V = 1,375.22,4 = 30,8 (lít)


bạn nào cò lời giải khác không a