Một hỗn hợp X gồm ancol no đơn chức A và axit no đơn chức B chia làm 2 phần bằng nhau. Phần 1 đem đốt hoàn toàn thu được 0,1 mol CO2. Phần 2 đem este hóa hoàn toàn thu được 1 este, đốt hết este thu được a gam nước. Tìm a?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án: D
Este tạo bởi ancol no đơn chức và axit no, đơn chức (tỷ lệ mol 1 : 1) nên este cũng no, đơn chức, có số mol bằng số mol ancol và axit (với hiệu suất 100%).
Đốt cháy este được nCO2 : nH2O
Áp dụng bảo toàn nguyên tố C có lượng CO2 thu được khi đốt cháy hỗn hợp A cũng tương đương lượng CO2 thu được khi đốt cháy este
=>nH2O = 0,8.0,1 = 0,08 mol => m = 1,44 gam

Phần 1: nancol = nH2O – nCO2 = 0,05
Phần 2: Ta thấy, lượng H2O loại đi chính là số mol este tạo thành
→neste = 0,25 – 0,22 = 0,03
→H = 0,3/0,5 = 60%
→ Đáp án D

Đáp án D
Phần 1:
![]()
Phần 2:
Ta thấy lượng H2O loại đi chính là số mol este tạo thành
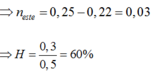

Chọn đáp án D
Phần 1:
![]()
Phần 2:
Ta thấy, lượng H2O loại đi chính là số mol este tạo thành
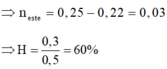

Este thu được sẽ là este no, đơn chức mạch hở
Khi đốt este này thì thu được nH2O = nCO2
Do số C không đổi trong cả 2 phần nên nH2O = 0,3 → mH2O = 5,4
→ Đáp án C

Đáp án: C
Vì ancol và axit được este hóa vừa đủ => nancol = naxit = x mol
Vì ancol no, đơn chức => khi đốt tạo ra nH2O - nCO2 = x
Vì axit no đơn chức => khi đốt tạo nH2O = nCO2
=> Nếu đốt trực tiếp X => nH2O = nCO2 + x = 0,3 + x mol
Sau phản ứng este hóa, có x mol H2O bị loại ra từ X
=> Lượng nước khi đốt este là : (0,3 + x) - x = 0,3 mol
=> mH2O = 0,3.18 = 5,4g

Đáp án: C
Dễ dàng thấy, nCO2 (1) = nCO2(2) = 0,3 mol
Mà ở phần 2, este tạo thành là no, hở đơn chức
=> nH2O = nCO2 = 0,3 mol
=> mH2O = 0,3.18 = 5,4 g

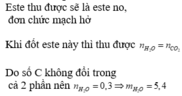
ancol; CnH2n+1OH
axit CmH2m+1COOH
đốt cháy; nCO2 =0,1
este hóa CnH2n+1OH + CmH2m+1COOH = CmH2m+1COOCnH2n+1 +H2O
đốt cháy este thu được 1 este
nH2O = (m+n+1). n(este) = nCO2 = nCO2(đốt cháy X) = 0,1
Vậy a=0,1.18=1,8 (g)