1 loại khí Cl2 chứa 2 đồng vị 35Cl và 37Cl, cho tác dụng với H2 rồi lấy sản phẩm hòa tan vào H2O thu được dung dịch A. Chia A thành 2 phần bằng nhau. Để trung hòa phần 1 cần dùng 125 ml dung dịch Ba(OH)2 0,88M. Phần 2 tác dụng với dung dịch AgNO3 dư thu được 31,57g kết tủa. Tính % mỗi loại đồng vị.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi phần trăm số nguyên tử của C 17 35 l là x, C 17 37 l là (100 – x).
Cl2 + H2 ® 2HCl (1)

M ¯ C l = 35 x + 37 ( 100 − x ) 100 ⇒ x = 75
Vậy thành phần phần trăm mỗi loại đồng vị của clo là : C 17 35 l (75% ) ; C 17 37 l (25%).
ĐÁP ÁN A

Đáp án D
Gọi phần trăm số nguyên tử của X 17 35 là x, X 17 37 là (100 – x).
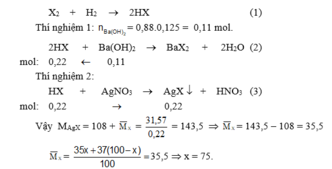
Vậy thành phần phần trăm mỗi loại đồng vị của clo là : C 17 35 l (75% ) ; C 17 37 l (25%).

Phần 1:
Đặt `n_{NaHCO_3}=x(mol);n_{Na_2CO_3}=y(mol)`
`->84x+106y={7,6}/2=3,8(1)`
`10ml=0,01l;300ml=0,3l`
`n_{HCl\ bd}=0,3.0,3=0,09(mol)`
`NaHCO_3+HCl->NaCl+CO_2+H_2O`
`Na_2CO_3+2HCl->2NaCl+CO_2+H_2O`
`NaOH+HCl->NaCl+H_2O`
Theo PT: `n_{HCl\ du}=n_{NaOH}=0,01.3=0,03(mol)`
`->n_{HCl\ pu}=x+2y=0,09-0,03=0,06(2)`
`(1)(2)->x=0,02(mol);y=0,02(mol)`
`->` Hỗn hợp ban đầu có \(\begin{cases}m_{NaHCO_3}=0,02.84.2=3,36(g)\\ m_{Na_2CO_3}=7,6-3,36=4,24(g)\end{cases}\)
Phần 2:
`NaHCO_3+Ca(OH)_2->CaCO_3+NaOH+H_2O`
`Na_2CO_3+Ca(OH)_2->CaCO_3+2NaOH`
Theo PT: `n_{CaCO_3}=x+y=0,04(mol)`
`->m_{\downarrow}=m_{CaCO_3}=0,04.100=4(g)`

\(n_{H_2}=\dfrac{1}{22,4}=\dfrac{5}{112}\left(mol\right)\)
\(n_{Cl_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: H2 + Cl2 --as--> 2HCl
Xét tỉ lệ: \(\dfrac{\dfrac{5}{112}}{1}>\dfrac{0,03}{1}\) => Hiệu suất tính theo Cl2
\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
Bảo toàn Cl: \(n_{Cl_2\left(pư\right)}=0,025\left(mol\right)\)
\(H\%=\dfrac{0,025}{0,03}.100\%=83,33\%\)

a)2Al+6HCl→2AlCl3+3H2
Fe+2HCl→FeCl2+H2
2Al+6H2SO4→Al2(SO4)3+3SO2+6H2O
2Fe+6H2SO4→Fe2(SO4)3+3SO2+6H2O
Cu+2H2SO4→CuSO4+SO2+2H2O
hh:Al(amol),Fe(bmol),Cu(cmol)
nNaOH=0,2×2=0,4mol
nHCl=0,4×2=0,8mol
⇒nHClpu=0,8−0,4=0,4mol
nSO2=5,6\22,4=0,25mol
27a+56b+64c=14,2
0,5a×3+0,5b×2=0,4
0,5a×1,5+0,5b×1,5+0,5c=0,25
⇒a=0,2;b=0,1;c=0,05
mAl=0,2×27=5,4g
mFe=0,1×56=5,6g
mCu=0,05×64=3,2g
b)mddspu=7,1+50−0,25×64=41,1g
C%Al2(SO4)3=41,6%
C%Fe2(SO4)3=24,33%
C%CuSO4=9,73%

\(n_{AgCl}=\dfrac{7,175}{143,5}=0,05\left(mol\right)\)
PTHH: HCl + AgNO3 ---> AgCl↓ + HNO3
0,05<---------------0,05
\(\rightarrow m_{HCl}=0,05.36,5=1,825\left(g\right)\\
\rightarrow C\%_{ddA}=\dfrac{1,825}{50}.100\%=3,65\%\)
\(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Đặt H = x%
PTHH: Cl2 + H2 --as--> 2HCl
LTL: 6,72 < 10 => H2 dư
=> nHCl = 0,3x (mol)
\(\rightarrow C\%_{HCl}=\dfrac{0,3x.36,5}{0,3x.36,5+385,4}.100\%=3,65\%\\ \Leftrightarrow20,23\%\)

Đáp án A
P1: nFe(OH)2 = 3,6/90 = 0,04 mol => nFe2+ = 0,04 mol
P2:
Fe2+: x mol
H+: y mol
Cl-: 2x + y
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
0,06 ← 0,08 ← 0,02
=> y = 0,08
Fe2+ + Ag+ → Fe3+ + Ag
x-0,06 → x-0,06
Ag+ + Cl- → AgCl
2x+y → 2x+y
=> 108(x-0,06) + 143,5(2x+y) = 68,2 => x = 0,16
=> nFe phản ứng ban đầu = nH2 = 0,04+0,16 = 0,2 mol => VH2 = 4,48 lít



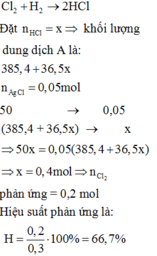
Gọi phần trăm số nguyên tử của \(^{35}Cl\) là x, \(^{37}Cl\)là (100 – x).
Cl2 + H2 ------> 2HCl (1)
\(\overline{M_{Cl}}=\dfrac{35x+37\left(100-x\right)}{100}=35,5\)
=> x = 75
Vậy thành phần phần trăm mỗi loại đồng vị của clo là : 35Cl(75% ); 37Cl(25%).