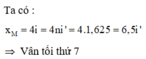Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

tìm khối lượng mol của các chất khí sau so với CH4 có tỉ khối lần lượt là 2; 1,625 ; 0,125 và 1,0625

$M_{CH_4} = 16(đvC)$
Suy ra :
$M_1 = 16.2 = 32(đvC)$
$M_2 = 16.1,625 = 26(đvC)$
$M_3 = 16.0,125 = 2(đvC)$
$M_4 = 16.1,0625 = 17(đvC)$

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,9}{18}=0,05\left(mol\right)\)
Bảo toàn C: nC = 0,1 (mol)
Bảo toàn H: nH = 0,1 (mol)
Xét mC + mH = 12.0,1 + 1.0,1 = 1,3 (g)
=> A chứa C và H
Xét nC : nH = 0,1 + 0,1 = 1 : 1
=> CTPT: (CH)n
Mà MA = 1,625.16 = 26 (g/mol)
=> n = 2
=> CTPT: C2H2

\(n_{Zn}=\dfrac{1,625}{65}=0,025mol\)
\(n_{HCl}=\dfrac{3,65}{36,5}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,025 < 0,1 ( mol )
0,025 0,05 0,025 0,025 ( mol )
\(V_{H_2}=0,025.22,4=0,56l\)
Chất dư là HCl
\(m_{HCl\left(dư\right)}=\left(0,1-0,05\right).36,5=1,825g\)
\(m_{ZnCl_2}=0,025.136=3,4g\)
huhu cảm ơn bạn đề dài quá nên đưa lên đây làm giúp

a, Ta có: \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
⇒ mC + mH = 0,4.12 + 0,4.1 = 5,2 (g) = mA
Vậy: A chỉ chứa C và H.
Gọi CTPT của A là CxHy.
⇒ x:y = 0,4:0,4 = 1:1
→ CTPT của A có dạng là (CH)n.
Mà: \(M_A=1,625.16=26\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{26}{12+1}=2\)
Vậy: CTPT của A là C2H2.
b, CTCT: \(CH\equiv CH\)
- Tchh đặc trưng: tham gia pư cộng, pư thế ion kim loại.
- Điều chế: \(2CH_4\underrightarrow{1500^o}C_2H_2+3H_2\)
\(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)