Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích các bước giải:
Ca3(PO4)2 + 5C+ 3SiO2 --> 5CO + 2P + 3CaSiO3
P +O2--> P2O5
P2O5 + 3H2O --> 2H3PO4
H3PO4 + 3NH3 --> (NH4)3PO4
2(NH4)3PO4+H2SO4( đặc) --> 3(NH4)2SO4+ 2H3PO4
2H3PO4+ 3CaS --> Ca3(PO4)2 + 3H2S

1. Phương trình hoá học tạo thành loại phân bón amophot phù hợp với đề bài :
![]()
2. Tính khối lượng amophot thu được :
Số mol
N
H
3
: 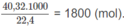
Số mol
H
3
P
O
4
: 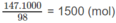
Tỉ lệ số mol NH3: số mol H 3 P O 4 = 1800 : 1500 = 6:5, vừa đúng bằng tỉ lệ hợp thức trong phương trình hoá học (1). Vậy lượng N H 3 phản ứng vừa đủ với lượng H 3 P O 4 . Do đó, có thể tính lượng chất sản phẩm thec N H 3 hoặc theo H 3 P O 4 .
Theo lượng
H
3
P
O
4
, số mol
N
H
4
H
2
P
O
4
: 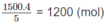
và số mol
(
N
H
4
)
2
H
P
O
4
: 
Khối lượng amophot thu được:
m N H 4 H 2 P O 4 + m ( N H 4 ) 2 H P O 4 = 1200.115 + 300.132 = 177,6.103 (g) hay 177,6 kg

2H3PO4 + 3Ca(OH)2 → Ca3(PO4)2 + 6H2O
2H3PO4 + 3Ca2+ + 6OH- → Ca3(PO4)2 + 6H2O

Phương trình hoá học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch :
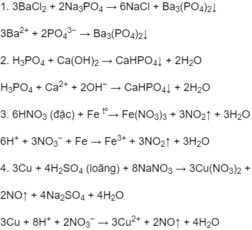

2H3PO4 + 3K2CO3 → 2K3PO4 + 3H2O + 3CO2↑
2H3PO4 + 3CO32- → 2PO43- + 3H2O + CO2↑

Các chất lấy dư nên muối tạo ra là muối trung hoà: 2H3PO4 + 3BaO → Ba3(PO4)2 + 3H2O
Phương trình phân tử trùng với phương trình ion thu gọn

(1) sai, khoáng vật chính của photpho trong tự nhiên là apatit và photphorit
(2) đúng
(3) đúng
(4) sai, trong phòng thí nghiệm, axit photphoric được điều chế bằng phản ứng giữa P và
H
N
O
3
đặc
(5)sai, P hoạt động hơn N do N tồn tại ở
N
2
có liên kết ba bền
Đáp án B

- Những tính chất chung: Đều có tính axit
+ Chuyển màu chất chỉ thị: Quỳ tím chuyển thành màu hồng
+ Tác dụng với bazơ, oxit bazơ không có tính khử (các nguyên tố có số oxi hoá cao nhất):
3NaOH + H3PO4 → Na3PO4 + 3H2O
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
+ Tác dụng với một số muối của axit yếu và không có tính khử:
2HNO3 + CaCO3 → Ca(NO3)2 + H2O + CO2↑
2H3PO4 + 3Na2SO3 → 2Na3PO4 + 3H2O + 3SO2↑
- Những tính chất khác nhau:
| HNO3 | H3PO4 |
| - Axit HNO3 là axit mạnh HNO3 → H+ + NO3- - Axit HNO3 có tính oxi hoá mạnh Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O S + 2HNO3 → H2SO4 + 2NO 3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O |
- Axit H3PO4 là một triaxit trung bình H3PO4 ⇆ H+ + H2PO4- H2PO4- ⇆ H+ + HPO42- HPO42- ⇆ H+ + PO43- - Axit H3PO4 không có tính oxi hoá. 3Fe + 2H3PO4 → Fe3(PO4)2 + 3H2 S + H3PO4 → không phản ứng 3FeO +2H3PO4 → Fe3(PO4)2 + 3H2O |

Các phương trình hoá học thực hiện dãy chuyển hoá :