Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
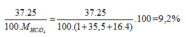

Tham thảo :
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4= 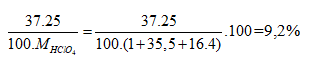

Đáp án D.
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4= 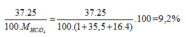

Đáp án D
Phần trăm khối lượng của C 37 l trong HClO4 là:
37 . 0 , 2423 1 + 35 , 5 + 64 . 100 % = 8 , 92 %

Đáp án A
Giả sử % nguyên tử 35Cl và 37Cl trong tự nhiên lần lượt là x, y.
Ta có hpt
x + y = 1 35 x + 37 y = 35 , 5
⇒ x = 0 , 75 y = 0 , 25
Phần trăm khối lượng của 37Cl trong HClO4 là
(0,24.37)/ (1+35,5+ 16.4) = 9,2 %
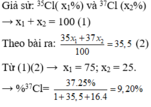
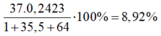
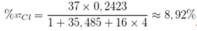
- Tính % số nguyên tử của hai đồng vị clo:
Gọi x là % số nguyên tử của 3717Cl và (100 - x) là % số nguyên tử của 3517Cl. Ta có: 37x + (100 – x).35 = 35,5.100 → x = 25%
Vậy 3717Cl chiếm 25% số nguyên tử và 3517Cl chiếm 75% số nguyên tử.
- Giả sử có 1 mol HClO4 thì có 1 mol clo, trong đó có 0,25 mol 3717Cl. Do đó, phần trăm khối lượng 3717Cl trong HClO4:
0,25 . 37 / 100,5 = 9,2 %
- Viết công thức electron đầy đủ và CTCT , xác định số oxi hóa của clo trong hợp chất là +7
uk