Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(m_{đường}=300.25\%=75\left(g\right)\\ \Rightarrow m_{H_2O}=300-75=225\left(g\right)\\ \Rightarrow V_{H_2O}=\dfrac{225}{1}=225\left(ml\right)\)
Cách pha chế: Lấy 75 gam đường và đong 225ml nước, sau đó khuấy đều cho đến khi đường tan hoàn toàn ta được 300g dung dịch đường nồng độ 25%

1) Thực hành 1
Phần tính toán
Khối lượng chất tan (đường) cần dùng là:
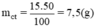
Khối lượng nước cần dùng là: 50 - 7,5 = 42,5(g).
Phần thực hành:
Cần 7,5g đường khan cho vào cốc có dung tích 100ml, khuấy đều với 42,5g nước, được 50g dung dịch đường 15%.
2) Thực hành 2
Phần tính toán
Số mol NaCl cần dùng là:
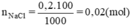
Có khối lượng là: 58,5 x 0,02 = 1,17(g).
Phần thực hành:
Cho 1,17g NaCl khan cho vào cốc chia độ. Rót từ từ nước vào cốc và khuấy đều đến cho vạch 100ml, được 100ml dung dịch NaCl 0,2M.
3) Thực hành 3
Phần tính toán
Khối lượng chất tan(đường) có trong 50g dung dịch đường 5% là:
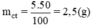
Khối lượng dung dịch đường 15% có chứa 2,5g đường là:
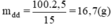
Khối lượng nước cần dùng là: 50 - 16,7 = 33,3(g).
Phần thực hành:
Cần 16,7g dung dịch đường 15% cho vào cốc có dung tích 100ml.Thêm 33,3g nước (hoặc 33,3ml) vào cốc, khuấy đều, được 50g dung dịch đường 5%.
4) Thực hành 4
Phần tính toán
Số mol chất tan (NaCl) có trong 50ml dung dịch 0,1M cần pha chế là:
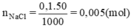
Thể tích dung dịch NaCl 0,2M trong đó có chứa 0,005mol NaCl là:
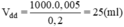
Phần thực hành:
Đong 25ml dung dịch NaCl 0,2M cho vào cốc chia độ. Rót từ từ nước vào cốc đến vạch 50ml. Khuấy đều, được 50ml dung dịch NaCl 0,1M.

a) n CuSO4 =0,4.0,05 = 0,02(mol)
=> V dd CuSO4 = 0,02/2 = 0,01(lít) = 10(ml)
=> V H2O thêm vào = 50 - 10 = 40(ml)
Pha chế : Đong lấy 40 ml nước cất cho vào 10 ml dung dịch CuSO4 2M, khuấy đều
b)
m NaCl = 50.2,5% = 1,25(gam)
m dd NaCl 10% = 1,25/10% = 12,5(gam)
=> m H2O cần thêm = 50 - 12,5 = 37,5 gam
- Cân lấy 12,5 gam dd NaCl 10%
- Đong lấy 37,5 gam nước cho vào cốc, khuấy đều.

 \(m_{NaCl}=\dfrac{2,5.150}{100}=3,75\left(g\right)\\
m_{\text{dd}}=\dfrac{100.3,75}{10}=37,5\left(g\right)\\
m_{H_2O}=150=37,5=112,5\left(g\right)\)
\(m_{NaCl}=\dfrac{2,5.150}{100}=3,75\left(g\right)\\
m_{\text{dd}}=\dfrac{100.3,75}{10}=37,5\left(g\right)\\
m_{H_2O}=150=37,5=112,5\left(g\right)\)
\(n_{NaCl}=0,05.2=0,1\left(mol\right)\\ m_{NaCl}=0,1.58,5=5,85\left(g\right)\)
cân lấy 5,85 g NaCl cho vào cốc thủy tính có dung tích 100ml ,đổ dần dần nước cất vào cốc và khuấy nhẹ cho đủ 50ml dd

khi trộn cát trăng với muối trộn đều cho nhau thì làm cách nào để lấy đc muôi bài 2 CHẤT

\(n_{H_2SO_4}=0.5\cdot1=0.5\left(mol\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.5\cdot98\cdot100}{98}=50\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{50}{1.84}=27.17\left(ml\right)=0.02717\left(l\right)\)

Gọi số ml dd HCl ở lọ 1 và 2 lần lượt là:a;b(ml)
V của dd HCl 1M là:a
V của dd HCl 3M là:3b
Ta có:
CM=\(\dfrac{a+3b}{a+b}=2\)(a+b=50)
\(\Leftrightarrow a+3b=100\)
\(\Leftrightarrow2b=50\)
\(\Leftrightarrow b=25\)
\(\Rightarrow a=25\)
Vậy để pha chế 50 ml dd HCl 2M thì ta cần đổ 25ml dd HCl 1M và 25ml dd HCl 3M
Gọi a, b lần lượt là thể tích dung dịch HCl của lọ thứ 1và lọ thứ 2 (a, b > 0 , lít)
=>: \(a+b=0,05\left(I\right)\)
Ta có: \(n_{HCl}\)(lọ 1) \(=a.1=a\left(mol\right)\)
\(n_{HCl}\)(lọ 2) \(=3b\left(mol\right)\)
\(n_{HCl}\left(sau\right)=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow a+3b=0,1\left(II\right)\)
Từ (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,025\left(lit\right)=25\left(ml\right)\\b=0,025\left(lit\right)=25\left(ml\right)\end{matrix}\right.\)
Vậy....
\(n_{NaCl}=0,5.0,4=0,2\left(mol\right)\Rightarrow m_{NaCl}=58,5.0,2=11,7\left(g\right)\\ V_{H_2O}=V_{ddNaCl}=500\left(ml\right)=0,5\left(l\right)\)
Pha chế: Đong 500ml H2O và cân 11,7 gam NaCl, sau đó đổ nước vào bình có chứa 11,7gam NaCl. Tiến hình hoà tan NaCl đến khi NaCl tan hết ta được 500ml dung dịch Natri Clorua có nồng độ 0,4M.