
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


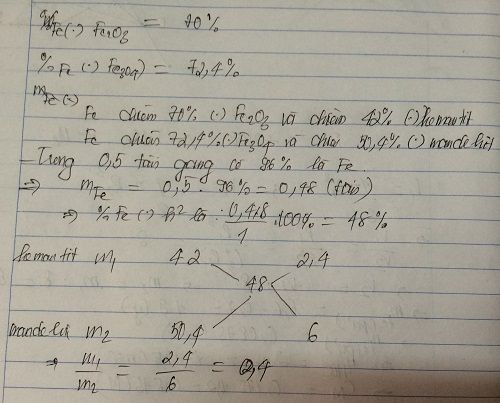
đề sai sai nha !
X là quặng hematit chứa 60% Fe2O3, Y là quặng manhetit chứa 69,6% Fe3O4. Cần trộn X, Y theo tỉ lệ khối lượng như thế nào để được quặng Z mà từ 1 tấn quặng Z có thể điều chế được 0,5 tấn gang chứa 96% sắt?OK!

trong gang:nFe =3/350
BT ng tu ngto:2nFe2O3+3nFe3O4=3/350
=>2*0.6*m1/160+3*0.696*m2/232=3/350
m1+m2=1
=>m1=2/7;m2=5/7
=>m1:m2=2/5

Vì lượng Fe hao phí 5% nên
=> mFe = \(\dfrac{1.\left(90+5\right)}{100}=0,95\left(tấn\right)\)
PTHH :
\(Fe2O3+3CO-^{t0}->2Fe+3CO2\uparrow\)
160 tấn ---------------------> 112 tấn
x tấn ----------------------> 0,95 tấn
=> x = \(\dfrac{0,95.160}{112}\approx1,357\left(tấn\right)\)
=> m(quặng) = \(\dfrac{1,357.100}{87}\approx1,56\left(tấn\right)\)

a)
\(n_{KClO_3}=\dfrac{24.5}{122.5}=0.2\left(mol\right)\)
\(2KClO_3\underrightarrow{^{^{t^0}}}2KCl+3O_2\)
\(n_{O_2}=\dfrac{3}{2}\cdot0.2=0.3\left(mol\right)\)
\(V_{O_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(n_{O_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
\(0.2...............................................0.1\)
\(n_{KMnO_4\left(bđ\right)}=\dfrac{0.2}{90\%}=\dfrac{2}{9}\left(mol\right)\)
\(m_{KMnO_4}=\dfrac{2}{9}\cdot158=35.11\left(g\right)\)


12.6 tấn sắt = 12600 kg
MFe3O4 = 56*3 + 16*4= 232 (g/mol)
Trong 232 g Fe3O4 có 168 g Fe
x g Fe3O4 (= 12600 g Fe
mFe304 = x = 12600*232 : 168 = 17400 (kg)
KL quặng sắt chứa 69,6% Fe304 là
17400 * 100 : 69.6 = 25000 (kg)
12.6 tấn sắt = 12600 kg
MFe3O4 = 56*3 + 16*4= 232 (g/mol)
Trong 232 g Fe3O4 có 168 g Fe
x g Fe3O4 (= 12600 g Fe
mFe304 = x = 12600*232 : 168 = 17400 (kg)
KL quặng sắt chứa 69,6% Fe304 là
17400 * 100 : 69.6 = 25000 (kg)