Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi số mol Mg, Fe là a, b (mol)
=> 24a + 56b = 8 (1)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a-->2a---------------->a
Fe + 2HCl --> FeCl2 + H2
b--->2b---------------->b
=> a + b = 0,2 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1.24}{8}.100\%=30\%\\\%m_{Fe}=\dfrac{0,1.56}{8}.100\%=70\%\end{matrix}\right.\)
b) nHCl = 2a + 2b = 0,4 (mol)
=> \(V_{dd.HCl}=\dfrac{0,4}{2}=0,2\left(l\right)\)

Đáp án C
Gọi M là kim loại nhóm II, số mol là x
M + 2HCl " MCl2 + H2
x(mol) x(mol)
Theo đề bài ra ta có hệ phương trình: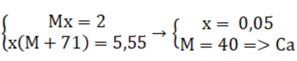

Đáp án B
Ta có n H 2 = P V R T = 1 . 6 , 11 22 , 4 273 ( 273 + 25 ) = 0 , 25 m o l
Gọi A là kí hiệu, nguyên tử khối của kim loại.
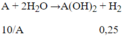
⇒10/A= 0,24 →A = 40 (Ca)

Đáp án B
Phương trình phản ứng
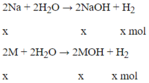
Theo đề bài ta có: 23x +Mx = 6,2 (1)
Áp dụng định luật bảo toàn khối lượng ta có:
mkim loại + mnước = mdd + mhiđro
Từ đó: mhiđro = mkim loại - mnước = mdd = 6,2 + 104 - 110 = 0,2 (g)
⇒x = 0,1 mol, thay vào (1) ta được M = 39 (K)

Đáp án B
1-đúng, Cr bị thụ động.
2-sai, CrO3 là oxit axit.
3-đúng.
4-sai, Cr tác dụng với Cl2 tạo ra CrCl3.
5-đúng.
6-sai, Cr hoạt động mạnh hơn Fe.
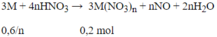
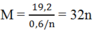
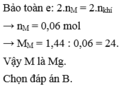
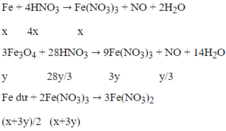
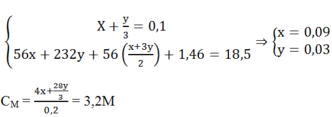
Văn vở quá =))
Gọi công thức trung bình của 2 kim loại là R ( R hóa trị II)
PTHH : R + 2HCl → RCl2 + H2
nH2 = \(\dfrac{4,032}{22,4}\)= 0,18 mol . Theo tỉ lệ phản ứng => nR = 0,18 mol
<=> MR = \(\dfrac{5,28}{0,18}\)= 35,2 (g/mol) => 2 kim loại là Mg và Ca
Gọi số mol Mg và Ca lần lượt là x và y mol ta có hệ pt:
\(\left\{{}\begin{matrix}x+y=0,18\\24x+40y=5,28\end{matrix}\right.\)=> x = 0,12 và y = 0,06
=> %mMg = \(\dfrac{0,12.24}{5,28}.100\)= 54,54% => %mCa = 100 - 54,54 = 45,46%