Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
Nhỏ từ từ đến lúc vừa hết 0,3 mol HCl thì thấy đã dùng 2x mol KHCO3 và x mol K2CO3
Phản ứng: KHCO3 + HCl → KCl + CO2 + H2O || K2CO3 + 2HCl → 2KCl + CO2 + H2O
⇒ 2x + 2 × x = ∑nHCl phản ứng = 0,3 mol ⇒ x = 0,075 mol
⇒ ∑nCO2 = 3x = 0,225 mol ⇒ VCO2 = 0,225 × 22,4 = 5,04 lít. Chọn B

Đáp án A
nOH- = 0,1.2 + 0,225 + 0,2 = 0,625 mol
Do nH+>nCO2 nên X có cả CO32- => X không có Ba2+ => nBaCO3 = 0,1 mol
Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+
x+y = nCO2 = 0,25
2x+y = nH+ = 0,35
=> x = 0,1; y = 0,15
Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (0,1k mol), HCO3- (0,15k mol)
BTĐT: 0,225 + 0,2 = 2.0,1k + 0,15k => k = 1,3
BTNT C: nCO2 ban đầu = nBaCO3 + nCO32- + nHCO3- = 0,1 + 0,13 + 0,195 = 0,425 mol
=> V = 9,52 lít

Định hướng tư duy giải
Từ các đáp án → dung dịch chỉ có K+ và Na+
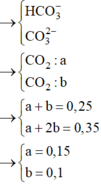
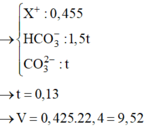

Đáp án A
Do 2 cách cho thì lượng khí CO2 thu được khác nhau nên HCl không dư.
Khi ta cho dung dịch Y từ từ vào X thì: n C O 2 = n H C l = n N a C O 3 = b - a m o l
Khi cho từ từ X tác dụng với Y thì hai muối trong X phản ứng theo tỉ lệ mol là 1:2.
Phản ứng: N a 2 C O 3 + 2 K H C O 3 + 4 H C l → 2 N a C l + 2 K C l + 3 C O 2 + 3 H 2 O
Lúc này: n C O 2 = 0 , 75 b
Từ giả thuyết suy ra: 0,75a=3(b-a)=> 3a= 2,25b=> a:b= 3:4
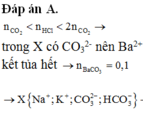
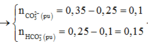
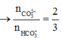


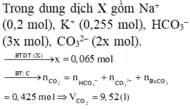
Đáp án B
(*) Phương pháp: Muối Cacbonat, Hidrocacbonat+ H +
-TH: Nếu cho từ từ muối ( C O 3 2 - : x mol và H C O 3 - : y mol) vào dung dịch axit
⇒ Do ban đầu H + rất dư so với muối nên 2 muối đều phản ứng đồng thời
C O 3 2 - + 2 H + → C O 2 + H 2 O
H C O 3 - + H + → C O 2 + H 2 O
-Lời giải: