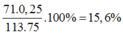Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Đặt mtơ tằm = x; mlông cừu = y ⇒ mhỗn hợp = a + b = 200(g).
mglyxin = 0,436x + 0,066y = 31,7(g) ||⇒ giải hệ cho: x = 50(g); y = 150(g).
► %mtơ tằm = 50 ÷ 200 × 100% = 25%

Gọi số mol Zn, AL là a, b (mol)
=> 65a + 27b = 3,79 (1)
\(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
a---->a------------------->a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b---->1,5b-------------------->1,5b
=> a + 1,5b = 0,08 (2)
(1)(2) => a = 0,05; b = 0,02
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,05.65}{3,79}.100\%=85,752\%\\\%m_{Al}=\dfrac{0,02.27}{3,79}.100\%=14,248\%\end{matrix}\right.\)
\(n_{H_2SO_4}=a+1,5b=0,08\left(mol\right)\)
=> \(m_{H_2SO_4}=0,08.98=7,84\left(g\right)\)
Zn + H2SO4 -> ZnSO4 + H2
a -> a
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
b -> 1.5b
HPT: 65a+27b=3.79
a + 1.5b = 1.792/22.4= 0.08
Giải HPT ta được a=0.05 b=0.02
mZn = 0.05*65=3.25 (g)
mAl= 0.02*27=0.54 (g)

\(n_{SO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
PTHH: \(2Al+6H_2SO_4\underrightarrow{t^o}Al_2\left(SO_4\right)_3+3SO_2+6H_2O\\ Mg+2H_2SO_4\underrightarrow{t^o}MgSO_4+SO_2+2H_2O\)
Đặt \(n_{Al}=a\left(mol\right);n_{Mg}=b\left(mol\right)\)
Ta có \(\left\{{}\begin{matrix}27a+24b=7,65\\1,5a+b=0,375\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,15\\b=0,15\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{27.0,15}{7,65}.100\%=52,94\%\\ \%m_{Mg}=100\%-52,94\%=47,06\%\)

\(n_{SO2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
Pt : \(Cu+2H_2SO_{4đặc}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
a 0,15 1a
\(2Fe+6H_2SO_{4đặc}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
b 0,075 1,5b
a) Gọi a là số mol của Cu
b là số mol của Fe
\(m_{Cu}+m_{Fe}=18\left(g\right)\)
⇒ \(n_{Cu}.M_{Cu}+n_{Fe}.M_{Fe}=18g\)
⇒ 64a + 56b = 18g (1)
Theo phương trình : 1a + 1,5b = 0,375(2)
Từ(1),(2), ta có hệ phương trình :
64a + 56b = 18g
1a + 1,5b = 0,375
⇒ \(\left\{{}\begin{matrix}a=0,15\\b=0,15\end{matrix}\right.\)
\(m_{Cu}=0,15.64=9,6\left(g\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
b) 0/0Cu = \(\dfrac{9,.6.100}{18}=53,33\)0/0
0/0Fe = \(\dfrac{8,4.100}{18}=46,67\)0/0
c) Có : \(n_{Cu}=0,15\left(mol\right)\Rightarrow n_{CuSO4}=0,15\left(mol\right)\)
\(n_{Fe}=0,15\left(mol\right)\Rightarrow n_{Fe2\left(SO4\right)3}=0,075\left(mol\right)\)
\(m_{CuSO4}=0,15.160=24\left(g\right)\)
\(m_{Fe2\left(SO4\right)3}=0,075.400=30\left(g\right)\)
Chúc bạn học tốt

Chọn đáp án B
Quy T về C2H3NO, CH2, H2O và (CH3COO)3C3H5 với số mol lần lượt là x, y, z và t.
mT = 57x + 14y + 18z + 218t = 31,88(g)
nNaOH = x + 3t = 0,44 mol.
● Muối gồm C2H4NO2Na, CH2 và CH3COONa
⇒ 97x + 14y + 82 × 3t = 41,04(g).
nO/T = 31,88 × 0,37139 ÷ 16
= 0,74 = x + z + 6t
⇒ Giải hệ có:
x = 0,2 mol; y = 0,14 mol; z = 0,06 mol; t = 0,08 mol
⇒ ktb = 0,2 ÷ 0,06 = 3,33.
||⇒ X là tripeptit và Y là tetrapeptit.
Giải hệ có: nX = 0,04 mol; nY = 0,02 mol.
nAla = nCH2 = 0,14 mol
⇒ nGly = 0,2 - 0,14 = 0,06 mol = 0,04 + 0,02
► X và Y đều chứa 1 Gly
⇒ Y là GlyAla3
⇒ %mY = 0,02 × 288 ÷ 31,88 × 100% = 18,07%.

Gọi a, b lần lượt là số mol của NaI và NaBr ban đầu, ta có : Sơ đồ phản ứng:
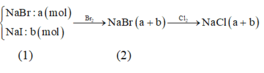

Đáp án A

Giải thích: Đáp án B
Xét trong 1 mol hỗn hợp :
- Gọi x là số mol MCl2 thì số mol của MSO4 là 1 - x
- Số mol của M : x + 1 - x = 1 mol
=> Khối lượng hỗn hợp là : (M + 71)x + (M + 96)(1 - x) = M + 96 - 25x
Phần trăm khối lượng M trong hỗn hợp là :
Ta có 0 < x < 1 => 18.9 < M < 25.7 => M = 24 (Mg)
=> x = 0.25 mol
=> khối lượng hỗn hợp là (24 + 71). 0,25 + (M + 96)(1 – 0,25) = 113.75g
=> %Cl =