Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`#3107.101107`
a.
Gọi số hạt proton, neutron, electron trong nguyên tử X lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử X là `48`
`=> p + n + e = 48`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 48`
Mà số hạt `p = n`
`=> 3p = 48`
`=> p = 48 \div 3`
`=> p = 16`
Vậy, số `p = n = e = 16`
b.
Khối lượng nguyên tử X là: `16 + 16 = 32` (amu)
c.
Bạn tham khảo mô hình NT X:
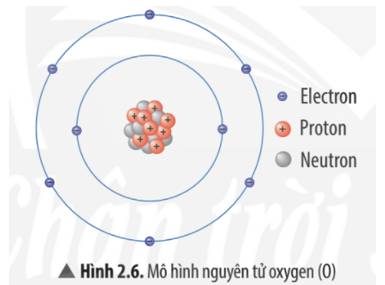
- X có `3` lớp electron
- X có `6` electron lớp ngoài cùng.

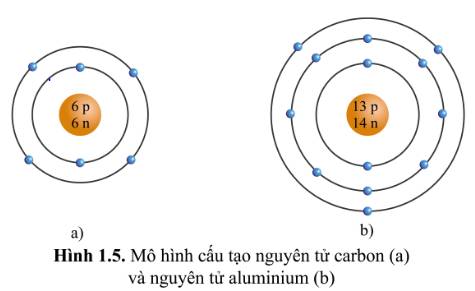
`a,` Carbon:
`p = 6 , e = 6 , n = 6`
`Alu``mi``nium:`
`p = 13 , n = 14 , e = 13`
`b,`Khối lượng nguyên tử của Carbon: `p+n = 6+6 = 12 <am``u>`
Khối lượng nguyên tử của Nhôm: `p+n = 13+14 = 27 <am``u>`

nguuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuu

Bạn kt lại đề xem có phải '' số hạt không mang điện tích ít hơn số hạt mang điện tích là 12" không nhe.
Ta có: P + E + N = 13
Mà P = E
=> 2P + N = 13 (1)
Có số hạt không mang điện tích ít hơn số hạt mang điện tích là 12:
Nên 2P \(-\) N = 12 (2)
Từ (1) và (2) ta có hệ phương trình
\(\left\{{}\begin{matrix}2P+N=13\\2P-N=12\end{matrix}\right.\)
=> P = E = 6,25
N = 0,5
Khối lượng X theo amu: 6,25.1+6,25.0,00055+0,5.1\(\approx\)6,75(amu)

Gọi p là số proton
Gọi n là số nơ tron
Gọi e là số electron
Theo đề bài ta có :
p+n+e=58 và p+n<40
Ta thấy p+n=39<40 (số khối hay Khối lượng nguyên tử) ⇒ n=58-39=19 electron (lớp 1 : 2 electron; lớp 2 : 8 electron; lớp 3: 8 electron; lớp 4 : 1 electron)
⇒ Nguyên tử đó có 4 lớp electron và lớp ngoài cùng có 1 electron ⇒ Thuộc chu kỳ 4 và Nhóm IA
Vậy nguyên tử đó là K (Protassium) và số hiệu nguyên tử là 19

Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2
Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2
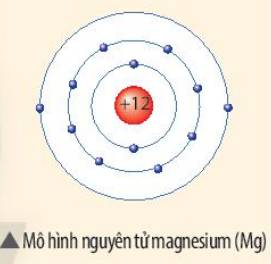

Một nguyên tử magnesium (Mg) gồm: 12 proton, 12 electron.
Khối lượng nguyên tử Mg bằng 12 + 12 = 24 amu.