Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) $n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
Theo PTHH : $n_{O_2} = \dfrac{3}{4}n_{Al} = 0,15(mol)$
$V_{O_2} = 0,15.22,4 = 3,36(lít)$
b) $2 KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,1(mol)$
$m_{KClO_3} = 0,1.122,5 = 12,25(gam)$
\(n_{Al}=\dfrac{m}{M}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ PTHH:4Al+3O_2-^{t^o}>2Al_2O_3\)
tỉ lệ: 4 : 3 : 2
n(mol) 0,2---->0,15---->0,1
\(V_{O_2\left(dktc\right)}=n\cdot22,4=0,15\cdot22,4=3,36\left(l\right)\\ PTHH:2KClO_3-^{t^o}>2KCl+3O_2\)
tỉ lệ: 2 : 2 : 3
n(mol) 0,1<-------------------------0,15
\(m_{KClO_3}=n\cdot M=0,1\cdot\left(39+35,5+16\cdot3\right)=12,25\left(g\right)\)

Bài 1: Số mol Al là 10,8/27=0,4 (mol).
4Al (0,4 mol) + 3O2 (0,3 mol) \(\underrightarrow{t^o}\) 2Al2O3.
a) Thể tích khí oxi cần dùng ở đktc là 0,3.22,4=6,72 (lít).
b) 2KMnO4 (0,6 mol) \(\underrightarrow{t^o}\) K2MnO4 + MnO2\(\downarrow\) + O2\(\uparrow\) (0,3 mol).
Khối lượng KMnO4 cần dùng là 0,6.158=94,8 (g).
Bài 2:
a) Fe2O3 (0,15 mol) + 3H2 (0,45 mol) \(\underrightarrow{t^o}\) 2Fe (0,3 mol) + 3H2O.
b) Khối lượng Fe2O3 cần dùng là 0,15.160=24 (g).
c) Thể tích khí hiđro đã dùng (đktc) là 0,45.22,4=10,08 (lít).
Bài 3: Số mol magie và axit sunfuric lần lượt là 3,6/24=0,15 (mol) và 24,5/98=0,25 (mol), H2SO4 dư.
Mg (0,15 mol) + H2SO4 (0,15 mol) \(\rightarrow\) MgSO4 + H2\(\uparrow\) (0,15 mol).
Thể tích khí hiđro thu được ở đktc là 0,15.22,4=3,36 (lít).
Bài 1:
Số mol của Al là:
nAl=10,8/27=0,4(mol)
PTHH: Al + O2 → Al2O3
0,4 → 0,4→ 0,4 (mol)
a)Thể tích của oxi ở đktc là:
VO2=0,4*22,4=8,96(l)
b) PTHH: 2KMnO4 → O2 + MnO2 + K2MnO4
0,8 0,4
Khối lượng của KMnO4 là:
mKMnO4=0,8*158=126,4(g)
Bài 2:
Số mol của sắt là:
nFe=16,8/56=0,3(mol)
a) PTHH: 4Fe + 3O2 → 2Fe2O3
0,3→0,225→ 0,15 (mol)
b) Khối lượng của Fe2O3 là:
mFe2O3=0,15*160=24(g)
c) Thể tích hidro cần dùng là:
VH2=0,225*22,4=5,04 (l)

\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
0,2 0,15 ( mol )
\(V_{O_2}=0,15.22,4=3,36l\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,3 0,15 ( mol )
\(m_{KMnO_4}=0,3.158=47,4g\)
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\
pthh:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,2 0,15
\(V_{O_2}=0,15.22,4=3,36l\\
PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,3 0,15
\(m_{KMnO_4}=158.0,3=47,4g\)

\(n_{Al}=\dfrac{5.4}{27}=0,2mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,2 0,15 0,1
a)\(V_{O_2}=0,15\cdot22,4=3,36l\)
b)\(n_{O_2}=0,15\cdot10\%=0,015mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,03 0,015
\(m_{KMnO_4}=0,03\cdot158=4,74g\)

nAl = 5,4/27 = 0,2 (mol)
PTHH: 4Al + 3O2 -> (t°) 2Al2O3
Mol: 0,2 ---> 0,15
VO2 = 0,15 . 22,4 = 3,36 (l)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,15 . 2 = 0,3 (mol)
mKMnO4 = 0,3 . 158 = 47,4 (g)

\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
\(0.2..........0.15\)
\(V_{O_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
\(0.3...............................................0.15\)
\(m_{KMnO_4}=0.3\cdot158=47.4\left(g\right)\)

PTHH : S + O2 → SO2
a) Áp dụng định luật bảo toàn khối lượng ta có:
\(m_S+m_{O_2}=m_{SO_2}\)
\(\Rightarrow m_{O_2}=m_{SO_2}-m_S=9,6-4,8=4,8\left(g\right)\)
b) \(n_{O_2}=\frac{m}{M}=\frac{4,8}{32}=0,15\left(mol\right)\)
\(\Rightarrow V_{O_2}=n.22,4=0,15.24=3,6\left(l\right)\)
c) \(V_{O_2}=V_{KK}.\frac{1}{5}\Rightarrow V_{KK}=V_{O_2}.5=3,6.5=18\left(l\right)\)
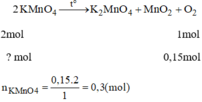
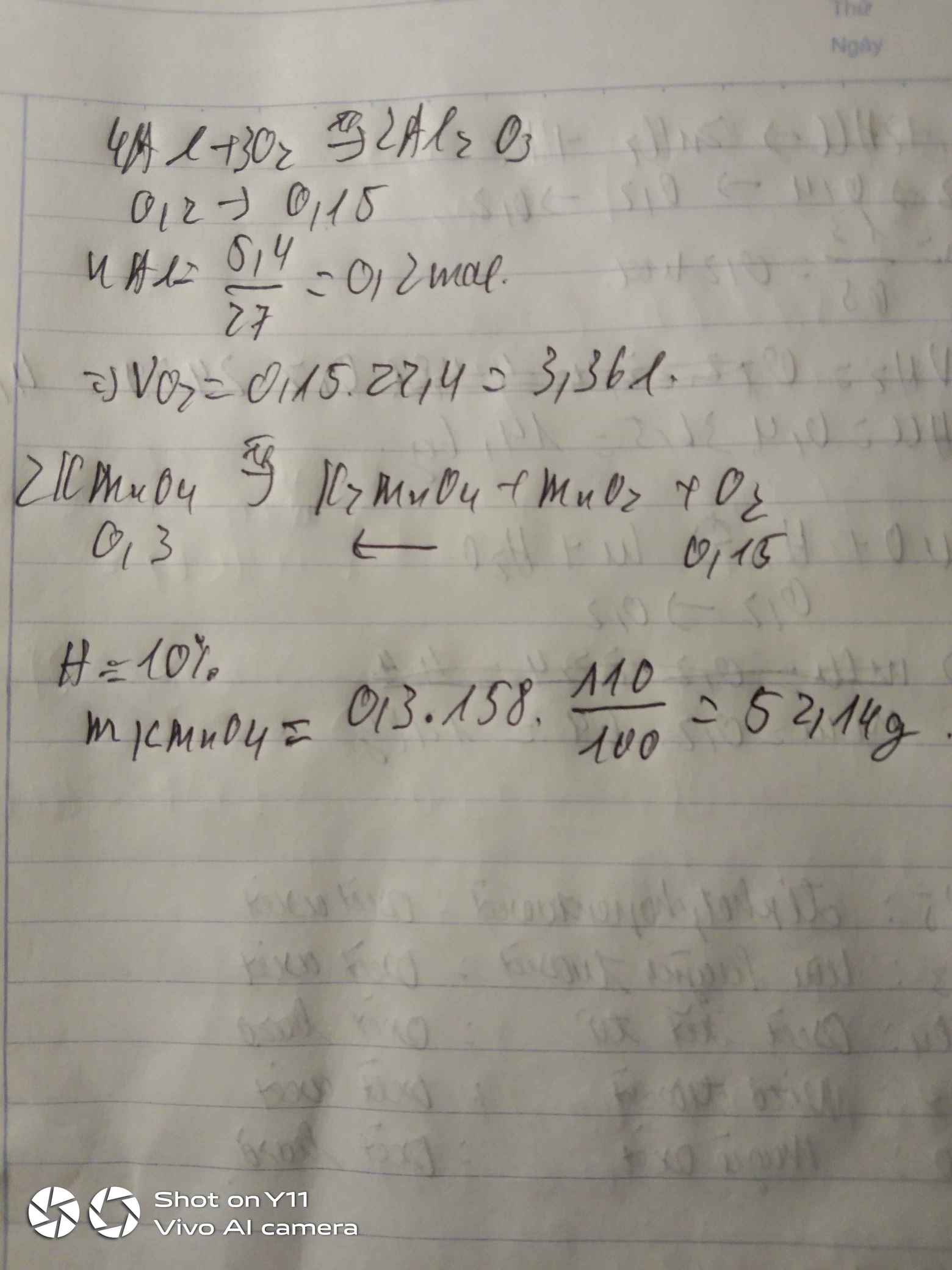
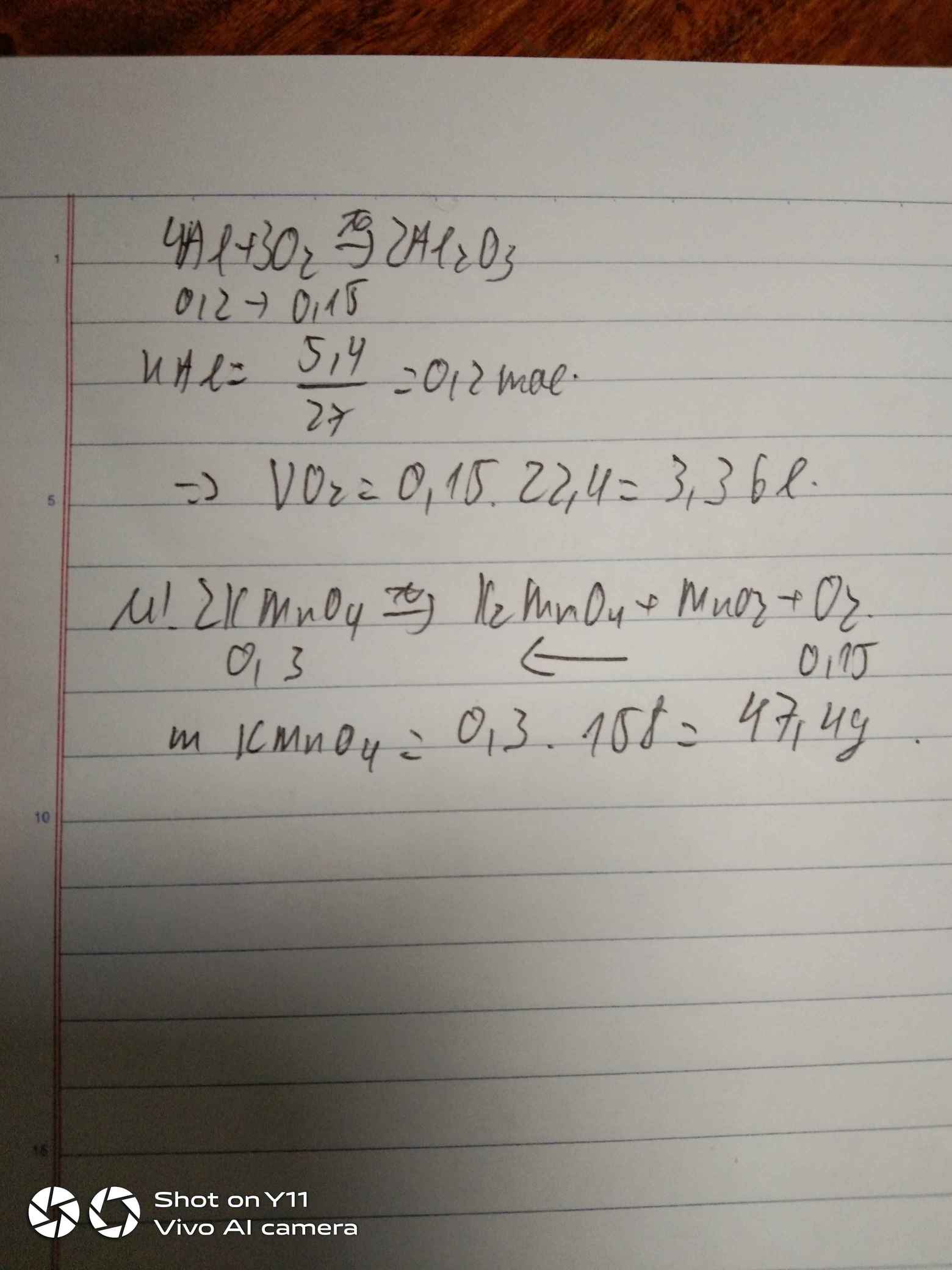
thank you nhé:>>