Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích các bước giải:
M Al2O3.SiO2.2H2O = 198
%mAl = = 27.2.100:198= 27,27%

Bài 4. Axit axetic có công thức C2H402. Hãy tính thành phần phần trăm khối lượng của các nguyên tố trong axit axetic.
Lời giải:
Từ C2H4O2 ta có: M = 60 g/mol; mC = 2 x 12 = 24 g; mH = 4 x 1 = 4 g;
MO = 2 x 16 = 32 g.
%C = (24 : 60) x 100% = 40%; %H = (4 : 60) x 100% = 6,67%;
%O = 100% - 40% - 6,67% = 53,33%.

Đun hỗn hợp với dung dịch NaOH đặc dư
SiO2 + 2NaOH ----> Na2SiO3 + H2O
Al2O3 + 2NaOH ---> 2NaAlO2 + H2O
Lọc tách phần dung dịch rồi dẫn khí CO2 tới dư vào
CO2 + NaOH ___> NaHCO3
CO2 + NaAlO2 + 2H2O--> Al(OH)3 ¯+ NaHCO3
Lọc tách kết tủa rồi nung ở nhiệt độ cao
2Al(OH)3 -----------> Al2O3 + 3H2O

nH2=0.56:22,4=0,025 mol
Fe+H2SO4----->FeSO4+H2
2AL+3H2SO4----->AL2(SO4)3 +3H2
Gọi x,y làn lượt là số mol Fe và AL
ta có hệ pt
\(\begin{cases}56x+27y=0,83\\x+1,5y=0,025\end{cases}\)
\(\begin{cases}x=0,01mol\\y=0,01mol\end{cases}\)
mFe=0,01.56=0,56 g
mAl=0,83-0,56=0,27 g
%mFe=(0,56:0,83).100=67,47%
%mAl=100-67,47=32,53%

mFe2O3 = 9.8%*100=9.8g mAl2O3= 10.2% *100=10.2g
=>mCaCO3 = 80g Theo đề, lượng chất rắn thu được sau khi nung chỉ bằng 67% lượng hỗn hợp ban đầu.Như vậy độ giảm khối lượng là do CO2 sinh ra bay đi.
mCO2=100-67=33g => nCO2= 33/44=0.75 mol
PTHH: CaCO3 ---t0---> CaO + CO2
0.75................0.75......0.75
mCaCO3=0.75*100=75g
Như vậy còn 5g CaCO3 còn dư. Do đó chất rắn tạo ra gồm:
CaCO3 dư, Al2O3, Fe2O3 và CaO.
%Al2O3= \(\dfrac{10.2}{67}\cdot100=15.22\%\)
%Fe2O3=\(\dfrac{9.8}{67}\cdot100=14.62\%\)
mCaO = 0.75*56=42g
=> %mCaO = 42%
mFe2O3 = 9.8%*100=9.8g mAl2O3= 10.2% *100=10.2g
=>mCaCO3 = 80g Theo đề, lượng chất rắn thu được sau khi nung chỉ bằng 67% lượng hỗn hợp ban đầu.Như vậy độ giảm khối lượng là do CO2 sinh ra bay đi.
mCO2=100-67=33g => nCO2= 33/44=0.75 mol
PTHH: CaCO3 ---t0---> CaO + CO2
0.75................0.75......0.75
mCaCO3=0.75*100=75g
Như vậy còn 5g CaCO3 còn dư. Do đó chất rắn tạo ra gồm:
CaCO3 dư, Al2O3, Fe2O3 và CaO.
%Al2O3= 10.267⋅100=15.22%10.267⋅100=15.22%
%Fe2O3=9.867⋅100=14.62%9.867⋅100=14.62%
%CaCO3dư = \(\dfrac{5}{67}\cdot100=7.4\%\)
=>%CaO=62.69%

Số mol C2H5OH = 9,2 : 46 = 0,2 (mol).
Phương trình phản ứng cháy :
C2H5OH + 3O2 -> 2CO2 + 3H2O.
0,2 0,6 0,4 mol
Thể tích khí CO2 tạo ra là : V = 0,4.22,4 = 8,96 (lít).
b) Thể tích khí oxi cần dùng là : V1 = 0,6 . 22,4 = 13,44 (lít).
Vậy thể tích không khí cần dùng là Vkhông khí = (lít).

Số mol hỗn hợp = 0m56 : 22,4 = 0,025 mol; số mol Br2 = 5,6 : 160 = 0,035 mol.
Gọi x, y lần lượt là số mol của etilen và axetilen.
a) Phương trình hoá học:
C2H4 + Br2 → C2H4Br2
P.ư: x x x (mol)
C2H2 + 2Br2 → C2H2Br4
P.ư: y 2y y (mol)
b) Ta có hệ phương trình: ; Giải hệ ta được y = 0,01 và x = 0,015
% =
x 100% = 60%;
= 100% - 60% = 40%

M Al2O3.2SiO2.2H2O =258
%mAl = \(\dfrac{54.100\%}{258}\)=20,93%
M Al2O3.2SiO2.2H2O =258
%mAl =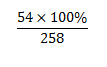 =20,93%
=20,93%