Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
xem dung dịch Y: bảo toàn 0,15 mol anion NO3–; Fe + Y → hỗn hợp kim loại + khí NO
||→ Y chứa cation Ag+ và H+. Quan sát sơ đồ bài tập HNO3:
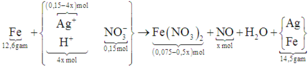
BTKL kim loại: 12,6 + 108 × (0,15 – 4x) = 56 × (0,075 – ½.x) + 14,5 ||→ x = 0,025 mol.
||→ ne trao đổi = nH+ sinh ra = 4z = 0,1 mol ||→ thời gian t = 96500 × 0,1 ÷ 2,68 = 3600 (s) ⇄ 1 giờ.
||→ theo đó đáp án cần chọn là C.

Đáp án B
4AgNO3 + 2H2O → d p 4Ag + 4HNO3 + O2
Dung dịch sau điện phân chứa AgNO3 dư = 0,3–x và HNO3 = x mol
Thấy mAg tối đa = 0,3 × 108 = 32,4 < 34,28g → chứng tỏ chất rắn chứa Ag :0,3-x và Fe dư :y
Có nNO = nHNO3 ÷ 4 = 0,25x mol
Bảo toàn electron → 2nFe pư = 3nNO + nAg.
⇒ nFe pư = ( 3×0,25x + 0,3-x) : 2 = 0,15-0,125x
→ 108×(0,3-x) + 22,4 – 56×(0,15-0,125x) = 34,28 ⇒ x = 0,12 mol
⇒ Thời gian điện phân t = 0 , 12 × 96500 2 , 68 × 3600 = 1,2 giờ

nAl=0,09 mol
nFe3O4=0,04\(\rightarrow\)nFe=0,12
Sau khi cho tác dụng với HCl thu được FeCl2 a mol FeCl3 b mol AlCl3 0,09 mol
Giải HPT: \(\left\{{}\begin{matrix}\text{2a+3b+0,09.3=0,62}\\\text{a+b=0,12}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}\text{a=0,01}\\\text{b=0,11}\end{matrix}\right.\)
Ta có Ag+ +Cl- \(\rightarrow\)AgCl
nAgCl=nCl=0,62 mol
Ag+ +Fe2+\(\rightarrow\)Fe3+ +Ag
nAg=nFeCl2=0,01
\(\rightarrow\)m=90,05

Đáp án A
Khối lượng dung dịch giảm gồm CuCl2: 0,075 mol và CuO : 14 , 125 - 0 , 075 . ( 64 + 71 ) 80 = 0,05 mol
Dung dịch Y chứa CuSO4 : 0,2- 0,075- 0,05 = 0,075 mol, H2SO4 : 0,125 mol ( bảo toàn nhóm SO42-)
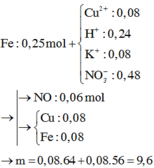
Khi cho 15 gam bột Fe thì xảy ra phản ứng
Fe + H2SO4 → FeSO4 + H2
Fe + CuSO4 → FeSO4 + Cu
Khối lượng chất rắn thu được gồm Cu : 0,075 mol và Fe dư: 15- 0,075. 56- 0,125. 56 = 3,8 gam.
⇒ m = 0,075. 64 +3,8 = 8,6 gam

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam




Chọn đáp án D