Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

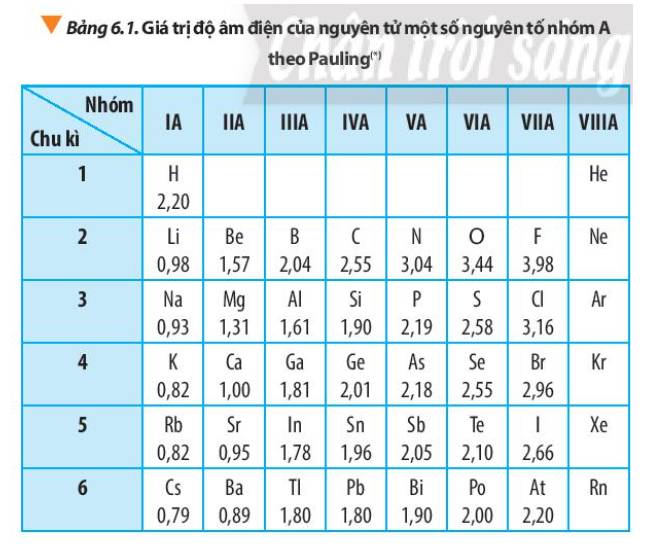
- Độ âm điện của nguyên tử các nguyên tố nhóm A có xu hướng biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân:
+ Trong một chu kì: theo chiều tăng dần của điện tích hạt nhân, lực hút giữa hạt nhân với các electron lớp ngoài cùng cũng tăng. Do đó, độ âm điện của nguyên tử các nguyên tố có xu hướng tăng dần
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử tăng nhanh, lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm. Do đó độ âm điện của nguyên tử các nguyên tố có xu hướng giảm dần

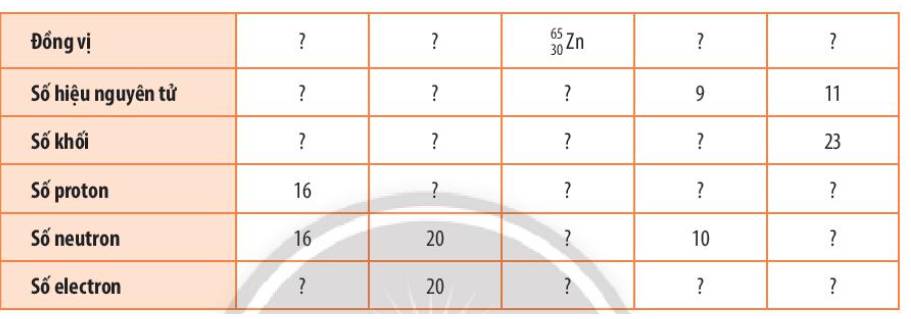
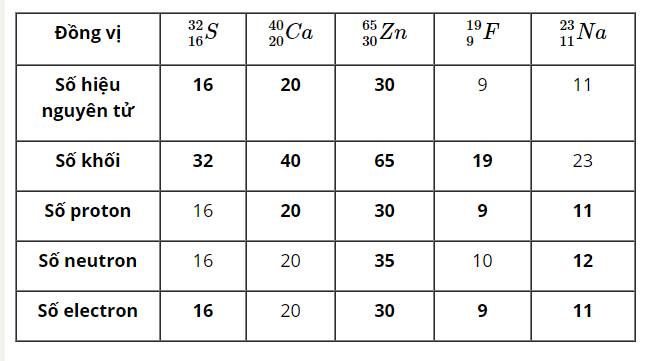
Hàng 1: \(^{32}_{16}S,^{40}_{20}Ca,^{65}_{30}Zn,^{19}_9F,^{23}_{11}Na\)
Hàng 2: 16, 20, 30, 8, 11
Hàng 3: 32, 40, 65, 18, 23
Hàng 4: 16, 20, 30, 9, 11
Hàng 5: 16, 20, 35, 10, 12
Hàng 6: 16,20,30,9,11

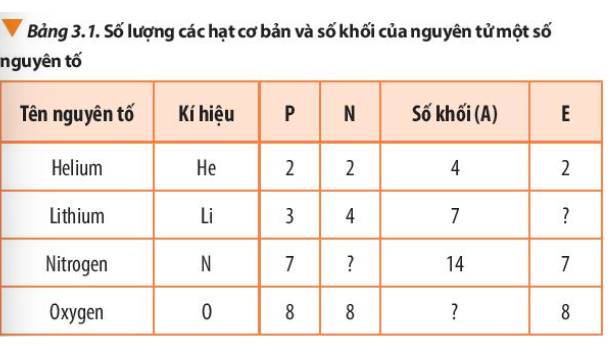
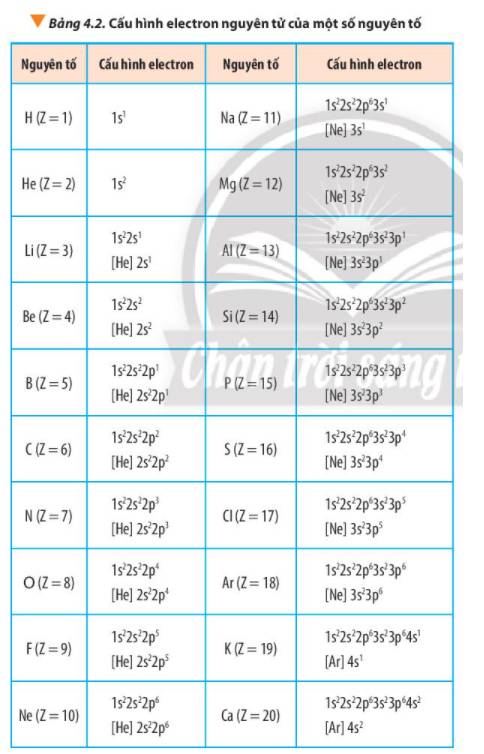
Số khối A = số proton (P) + số neutron (N)
Số electron (E) = Số proton (P)
Tên nguyên tố | Kí hiệu | P | N | Số khối (A) | E |
Helium | He | 2 | 2 | 4 | 2 |
Lithium | Li | 3 | 4 | 7 | 3 |
Nitrogen | N | 7 | 7 | 14 | 7 |
Oxygen | O | 8 | 8 | 16 | 8 |

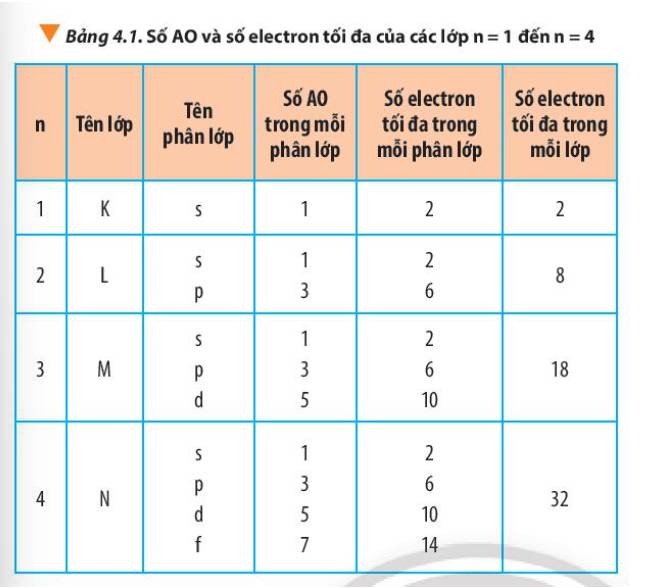
- Lớp 1 có tối đa 2 electron = 2.12
- Lớp 2 có tối đa 8 electron = 2.22
- Lớp 3 có tối đa 18 electron = 2.32
- Lớp 4 có tối đa 32 electron = 2.42
=> Số electron tối đa trong lớp n là 2n2

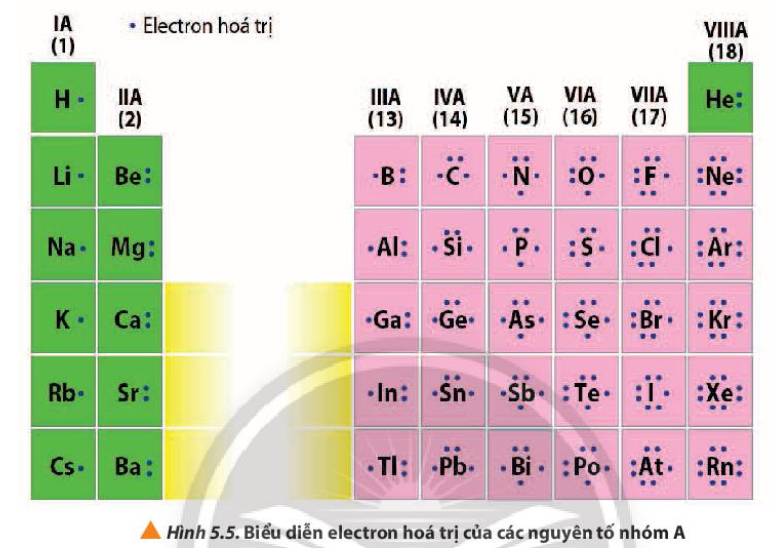
- Số electron hóa trị của nguyên tử = số thứ tự nhóm của nguyên tố nhóm A
Ví dụ:
+ Nhóm IA, các nguyên tố đều có 1 electron hóa trị
+ Nhóm IIIA, các nguyên tố đều có 3 electron hóa trị
+ Nhóm VIIIA (trừ He) các nguyên tố đều có 8 electron hóa trị


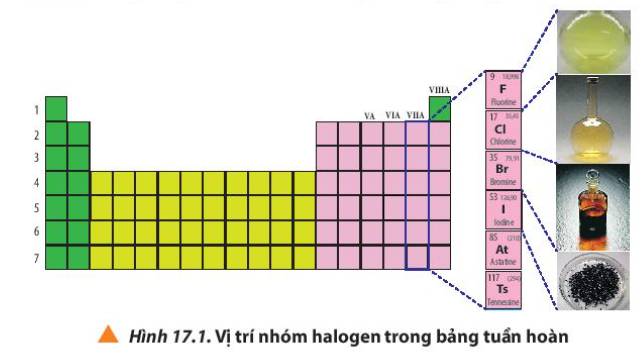
- Các nguyên tố nhóm VIIIA là các nguyên tố khí hiếm, bền ở điều kiện thường và không tham gia liên kết hóa học
=> Không hút electron vì cấu hình electron đã đạt cấu hình bền vững
=> Không có giá trị độ âm điện