
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


C2H5OH +O2 - lên men giấm -> CH3COOH +H2O (1)
Vrượu=\(\dfrac{20.15}{100}=3\left(l\right)\)=3000(ml)
=> mrượu =3000/0,8=3750(g)
theo (1) :
1 mol C2H5OH --> 1 mol axit
=> 46g C2H5OH --> 60g axit
3750 g C2H5OH --> x g axit
=>x=\(\dfrac{60.3750}{46}\approx4891,3\left(g\right)\)
mà H=90% => mCH3COOH (tt) =\(\dfrac{4891,3}{100}.90=4402,17\left(g\right)\)
=> mdd CH3COOH=\(\dfrac{4402,17.100}{2}=220108,5\left(g\right)=220,1085\left(kg\right)\)

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Gọi x, y , z lần lượt là số mol của Mg, Zn, Fe
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\) (1)
x -------> 2x--------->x------> x
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\) (2)
y ----> 2y -------->y --------> y
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (3)
z -----> 2z --------> z ----------> z
(1)(2)(3) \(\Rightarrow\left\{{}\begin{matrix}24x+65y+56z=21\\x+y+z=0,4\end{matrix}\right.\) (I)
\(2KOH+MgCl_2\rightarrow Mg\left(OH\right)_2\downarrow+2KCl\)
x ----------> x
\(2KOH+ZnCl_2\rightarrow Zn\left(OH\right)_2\downarrow+2KCl\)
\(2KOH+Zn\left(OH\right)_2\rightarrow K_2ZnO_2+2H_2O\) ( tan hết )
\(2KOH+FeCl_2\rightarrow Fe\left(OH\right)_2\downarrow+2KCl\)
z -----------> z
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\) (4)
x ----------------> x
\(2Fe\left(OH\right)_2+\dfrac{1}{2}O_2+H_2O\rightarrow2Fe\left(OH\right)_3\downarrow\)
z -------------------------------------> z
\(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H_2O\) (5)
z -----------------> 0,5z
(4)(5)\(\Rightarrow40x+160z=12\) (II)
(I)(II) \(\Rightarrow\left\{{}\begin{matrix}24x+65y+56z=21\\x+y+z=0,4\\40x+160.\dfrac{1}{2}z=12\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\\z=0,1\end{matrix}\right.\)
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(m_{Zn}=0,2.65=13\left(g\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
... Rồi xong, nếu em nộp bài trễ hơn một tí thì sửa được rồi . = . ....

a)
$Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
b)
$n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$m_{Zn} = 0,1.65 = 6,5(gam)$
$m_{ZnO} = 14,6 - 6,5 = 8,1(gam)$
c)
$n_{ZnO} = \dfrac{8,1}{81} = 0,1(mol)$
$n_{HCl} = 2n_{Zn} + 2n_{ZnO} = 0,4(mol)$
$\Rightarrow V_{dd\ HCl} = \dfrac{0,4}{C_{M_{HCl}}}$

a)
$Zn + 2HCl \to ZnCl_2 + H_2$
$ZnO + 2HCl \to ZnCl_2 + H_2O$
b)
Theo PTHH :
$n_{Zn} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$\Rightarrow m_{Zn} = 0,2.65 = 13(gam)$
$\Rightarrow m_{ZnO} = m_{hh} - m_{Zn} = 8,8 - 13 = -4,2 < 0$(Sai đề)

a)
Thể tích rượu etylic nguyên chất có trong 8l dd rượu là : VC2H5OH = \(\dfrac{8.5}{100}=0,4\left(l\right)\)
Khối lượng của rượu etylic là : m = D.V = 0,8.0,4.1000 = 320(g)
PTHH :
\(C2H5OH+O2-^{men,giấm}->CH3COOH+H2O\)
46g -----------------------------------> 60g
320g-----------------------------------> x g
=> x = 417,39(g)
Vì H = 8o% nên => mCH3COOH(thực tế) = \(\dfrac{417,39.80}{100}=333,912\left(g\right)\)
b) mdd(giấm) = \(\dfrac{333,912.100}{5}=6678,24\left(g\right)\)
a)
Thể tích rượu etylic nguyên chất có trong 8l dd rượu là : VC2H5OH = 8.5100=0,4(l)8.5100=0,4(l)
Khối lượng của rượu etylic là : m = D.V = 0,8.0,4.1000 = 320(g)
PTHH :
C2H5OH+O2−men,giấm−>CH3COOH+H2OC2H5OH+O2−men,giấm−>CH3COOH+H2O
46g -----------------------------------> 60g
320g-----------------------------------> x g
=> x = 417,39(g)
Vì H = 8o% nên => mCH3COOH(thực tế) = 417,39.80100=333,912(g)417,39.80100=333,912(g)
b) mdd(giấm) = 333,912.1005=6678,24(g)333,912.1005=6678,24(g)
Đúng 2 Bình luận Câu trả lời được cộng đồng lựa chọn Báo cáo sai phạm
Theo đề bài: cho A phản ứng với dung dịch NaOH thu được glixerol và 2 muối của 2 axit đơn chức, A chỉ chứa 1 loại nhóm chức
=> A là este 3 chức phản ứng với NaOH theo tỷ lệ mol 1:3 tạo ra 0,02 mol glixerol nên tiêu thụ 0,06 mol NaOH, tạo ra 0,04 mol 1 muối và 0,02 mol muối còn lại.
A + 3NaOH → C3H5(OH)3 + 2R1COONa + R2COONa
0,06 ← 0,02 → 0,04 → 0,02
=> nNaOH dư = 0,025.4 – 0,06 = 0,04 mol
Ta lại có: Axit X ít hơn Y 2 nguyên tử C và có cùng số nguyên tử H.
=> Gọi CTPT của các muối của X, Y với số mol tương ứng là CnHmCOONa x mol và Cn+2HmCOONa y mol.
Bảo toàn Na ta có:
nNa2CO3 = 1/2nNaOH bđ = 0,05 mol
Dẫn hỗn hợp khí và hơi sau khi đốt cháy B vào dung dịch Ba(OH)2 dư thì xảy ra phản ứng: Ba(OH)2 + CO2 → BaCO3 + H2O
=> nCO2 = nBaCO3 = 195,03/197 = 0,99 mol
Bảo toàn C ta có (n+1)x + (n+3)y = 0,05 + 0,99 =1,04 (*)
Xét 2 trường hợp có thể có với este A.
Trường hợp 1: A chứa 2 gốc axit X và 1 gốc axit Y
=> x = 0,04 mol, y = 0,02 thay vào (*) thì n = 15,67 vô lí (loại).
Trường hợp 2: A chứa 2 gốc axit Y và 1 gốc axit X
=> x = 0,02 mol, y = 0,04 mol thay vào (*) thì n =15
Khi đó 19,24 gam hỗn hợp B gồm: C15HmCOONa 0,02 mol, C17HmCOONa 0,04 mol và NaOH dư 0,04 mol.
=> 0,02(247 + m) + 0,04(271 + m) + 0,04 . 40 = 19,24
=> m = 31 (thỏa mãn)
=> 2 muối thu được là C15H31COONa và C17H31COONa
Este A có dạng:
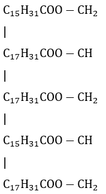
CTPT của A là C55H98O6

nZn= 19,5/65=0,3(mol); nFe2O3=19,2/160=0,12(mol)
PTHH: Zn + 2 HCl -> ZnCl2 + H2
Fe2O3 + 3 H2 -to-> 2 Fe +3 H2O
nH2=nZnCl2= nZn=0,3(mol) => V(H2,đktc)=0,3.22,4= 6,72(l)
b) nHCl= 2.0,3=0,6(mol) => mHCl=0,6.36,5=21,9(g)
=>mddHCl=(21,9.100)/20=109,5(g)
=>m=109,5(g)
c) mH2=0,3.2=0,6(mol)
mddZnCl2=19,5+109,5 - 0,6= 128,4(g)
mZnCl2=0,3. 136= 40,8(g)
=>C%ddZnCl2= (40,8/128,4).100=31,776%
d) Ta có: 0,3/3 < 0,12/1
=> H2 hết, Fe2O3 dư, tính theo nH2
=> nFe= 2/3. nH2= 2/3. 0,3= 0,2(mol)
=>mFe=0,2.56=11,2(g)
a, nZn = 19,5/65=0,3 (mol)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,3 0,15 0,3 0,3
=> \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b,mHCl=0,15.36,5=5,475 (g)
=> m=mddHCl=5,475:20%=27,375 (g)
c,mdd sau pứ =19,5+27,375=46,875 (g)
\(m_{ZnCl_2}=0,3.136=40,8\left(g\right)\)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{40,8}{46,875}.100\%=87,04\%\)
d,\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,3 0,2
Tỉ lệ: 0,12/1>0,3/3 ⇒ Fe2O3 dư,H2 pứ hết
=> mFe=0,2.56=11,2 (g)

Đáp án D.
Nhôm là kim loại có đủ các tính chất : nhẹ, dẫn điện, dẫn nhiệt, phản ứng mạnh với dung dịch axit clohiđric và tan trong dung dịch kiềm giải phóni: khí hiđro.
gvvvvvvvvvvvvvvvvvvvvvvvvvvft