Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nAg = 0,01 (mol)
NaX + AgNO3 →AgX + NaNO3
0,01 ← 0,01 (mol)
AgX →Ag
0,01 ← 0,01 (mol)
![]() , MX =80 (Br)
, MX =80 (Br)

nAg=0,01 mol
NaX+AgN03------->NaN03+AgX,áp dụng bảo toàn nguyên tố Ag,nAg sau=nAg truoc
0,01--------------------------------0,01
MNaX=1,03/0,01=103------------------->X=80------->Br

Chọn đáp án B
NaY + A g N O 3 → N a N O 3 + AgY
2AgY → 2Ag + Y 2
n N a Y = n A g Y = n A g = = 0,01 (mol)
=> 0,01(23 + M Y ) = 1,03 => M Y = 80 (Br)

nAg = 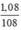 = 0,01 mol
= 0,01 mol
Phương trình hóa học của phản ứng:
Đặt X là kí hiệu, nguyên tử khối của halogen
NaX + AgNO3 → AgX↓ + NaNO3
0,01mol 0,01mol
2AgX → 2 Ag + X2
0,01mol 0,01mol
Theo pt: nNaX = nAgX = nAg = 0,1 mol
MNaX = 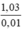 = 103 → X = 103 – 23 = 80 (Br)
= 103 → X = 103 – 23 = 80 (Br)
Muối A có công thức phân tử là NaBr

Chọn đáp án B
NaY + A g N O 3 → A g N O 3 + AgY
2AgY → 2Ag + Y 2
n N a Y = n A g Y = n A g = = 0,03 (mol
0,03(23+ M Y ) = 3,09 => M Y = 80 (Br)

a,
- Giả sử X là F (không tạo kết tủa) \(\Rightarrow\) Y là Cl.
\(AgNO_3+NaCl\rightarrow NaCl+AgNO_3\)
\(\rightarrow n_{NaCl}=n_{AgCl}=0,331\left(mol\right)\)
\(\Rightarrow m_{NaCl}=19,36< 22\left(g\right)\left(TM\right)\)
- Giả sử X, Y đều tạo kết tủa. Gọi chung là R.
nNaR= nAgR
\(\Rightarrow\frac{22}{23+R}=\frac{47,5}{108+R}\)
\(\Leftrightarrow47,5\left(23+R\right)=22\left(108+R\right)\)
\(\Leftrightarrow R=50,3\left(Cl;Br\right)\left(TM\right)\)
Vậy NaX, NaY có thể là NaF, NaCl hoặc NaCl, NaBr.
b,
- Trường hợp NaF, NaCl:
mNaCl= 19,36g
\(\Rightarrow C\%_{NaCl}=\frac{19,36.100}{200}=9,68\%\)
\(m_{NaF}=22-19,36=2,64\left(g\right)\)
\(\Rightarrow C\%_{NaF}=\frac{2,64.100}{200}=1,32\%\)
Trường hợp NaCl, NaBr
Gọi x là mol NaCl; y là mol NaBr
Bảo toàn nguyên tố, n muối= n kết tủa
\(\Rightarrow58,5x+103y=22;143,5x+188y=47,5\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(C\%_{NaCl}=\frac{0,2.58,5.100}{200}=5,85\%\)
\(C\%_{NaBr}=\frac{0,1.103.100}{200}=5,15\%\)

Gọi muối A có công thức tổng quát dạng NaX. ( X thuộc nhóm VIIA - halogen - là nguyên tử khối, là kí hiệu tổng quát)
PTHH: NaX+AgNO3→AgX+NaNO3 (1)
1(mol) --------------> 1(mol)
AgX→Ag+X (2)
1(mol)---> 1(mol)
Theo đề, ta có: nNaX=1,0323+X(mol);nAg=1,08/108=0,01(mol)
Theo 2 phương trình:nNaX=nAgX=nAg⇔1,0323+X=0,01⇔X=80
Vậy X là Br (Brom).
Vậy muối A là NaBr: Natri Bromua.
\(NaX+AgNO_3\rightarrow NaNO_3+AgX\)
\(2AgX\rightarrow2Ag+X_2\)
\(n_{Ag}=\frac{1,08}{108}=0,1\left(mol\right)\)
\(\rightarrow n_{NaX}=n_{Ag}=0,1\left(mol\right)\)
\(M_{NaX}=\frac{1,03}{0,01}=103\left(\frac{g}{mol}\right)\)
\(\rightarrow M_X=80\)
Vậy X là Brom