Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cách sắp xếp đúng là b): K, Na, Mg, Al.
Vì: - Các nguyên tố Na, Mg, AI ở cùng chu kì, theo chiều tăng dần điện tích hạt nhân, tính kim loại giảm. '
- Nguyên tố Na, K ở cùng một nhóm, theo chiều tăng điện tích hạt nhân, tính kim loại tăng.
Bài 5. Hãy cho biết cách sắp xếp nào sau đây đúng theo chiều tính kim loại giảm dần :
a) Na, Mg, Al, K ;
b) K, Na, Mg, Al;
c) Al, K, Na, Mg ;
d) Mg, K, Al, Na.
Giải thích sự lựa chọn.
Lời giải:
Cách sắp xếp đúng là b): K, Na, Mg, Al.
Vì: - Các nguyên tố Na, Mg, AI ở cùng chu kì, theo chiều tăng dần điện tích hạt nhân, tính kim loại giảm. '
- Nguyên tố Na, K ở cùng một nhóm, theo chiều tăng điện tích hạt nhân, tính kim loại tăng.

nA = = 0,015625 mol.
MA = = 64g
- Tìm số nguyên tử S, O trong phân tử A?
mO = 64 x = 32g => nO =
= 2 mol
mS = 64 - 32 = 32g => ns = = 1 mol
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO2
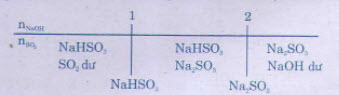
b) Khi dẫn SO2 vào dung dịch NaOH và SO2, có thể tạo thành muối trung hoà, muối axit hoặc cả hai muối:
Bài 7*. a) Hãy xác định công thức của hợp chất khí A, biết rằng :
- A là oxit của lưu huỳnh chứa 50% oxi.
- 1 gam khí A chiếm thề tích là 0,35 lít ở đktc.
b) Hoà tan 12,8 gam hợp chất khí A vào 300 ml dung dịch NaOH 1,2M. Hãy cho biết muối nào thu được sau phản ứng. Tính nồng độ mol của muối (giả thiết thể tích dung dịch thay đổi không đáng kể).
Lời giải:
nA = = 0,015625 mol.
MA = = 64g
- Tìm số nguyên tử S, O trong phân tử A?
mO = 64 x = 32g => nO =
= 2 mol
mS = 64 - 32 = 32g => ns = = 1 mol
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO2
b) * Hướng dẫn: Khi dẫn SO2 vào dung dịch NaOH và SO2, có thể tạo thành muối trung hoà, muối axit hoặc cả hai muối:


1. Phương trình phản ứng điều chế xút từ vôi sống và sô đa :
- CaO + H2O --> Ca(OH)2
- Ca(OH)2 + Na2CO3 --> CaCO3 + 2NaOH.
2. - Đặt công thức hóa học của kim loại cần tìm là: RO.
- Phương trình hóa học của phản ứng:
RO + 2HCl --> RCl2 + H2O
- Số mol axit HCl: nHClnHCl = 30.14,6100.36,530.14,6100.36,5 = 0,12 mol
- Số mol oxit : nROnRO = 0,12 : 2 = 0,06 mol
- Khối lượng mol của oxit là 4,8 : 0,06 = 80g
- PTK của oxit là RO = 80
- Nguyên tử khối của R bằng: 80 – 16 = 64 đvc.
Vậy R là Cu. Oxit cần tìm là CuO.
bài 1:
Phương trình phản ứng điều chế xút từ vôi sống và sô đa
- CaO + H2O \(\rightarrow\)Ca(OH)2
- Ca(OH)2 + Na2CO3 (sô đa) \(\rightarrow\) CaCO3 + 2NaOH.

Đối với chất khí, khi đo cùng diều kiện về nhiệt độ, áp suất thì trong phương trình hóa học, tỉ lệ vế số mol cũng là tỉ lệ về thể tích khí.
Khi dẫn hỗn hợp {CO, C02} qua nước vôi trong dư, toàn bộ CO2 bị hấp thụ hết do phản ứng với Ca(OH)2. Khí A là khí CO.
Phương trình hóa hóa học khi đốt khí CO:
O2 + 2CO 2CO2
p.ư: 2 → 4 lit
Trong 16 lít hỗn hợp {CO, C02} có 4 lít khí co và 16 - 4 = 12 lít khí CO2.
%VCO = 100% = 25%; % = 100% - 25% = 75%
Bài 5. Hãy xác định thành phần % về thể tích của mỗi khí trong hỗn hợp CO và CO2, biết các số liệu thực nghiệm sau :
a) Dần 16 lít hỗn hợp CO và CO2 qua nước vôi trong dư thu được khí A.
b) Để đốt cháy hoàn toàn khí A cần 2 lít khí oxi.
Các thể tích khí được đo ở cùng điểu kiện nhiệt độ và áp suất.
Lời giải:
Đối với chất khí, khi đo cùng diều kiện về nhiệt độ, áp suất thì trong phương trình hóa học, tỉ lệ vế số mol cũng là tỉ lệ về thể tích khí.
Khi dẫn hỗn hợp {CO, C02} qua nước vôi trong dư, toàn bộ CO2 bị hấp thụ hết do phản ứng với Ca(OH)2. Khí A là khí CO.
Phương trình hóa hóa học khi đốt khí CO:
O2 + 2CO 2CO2
p.ư: 2 → 4 lit
Trong 16 lít hỗn hợp {CO, C02} có 4 lít khí co và 16 - 4 = 12 lít khí CO2.
%VCO = 100% = 25%; % = 100% - 25% = 75%

a. \(n_{HCl}=\frac{44,8}{22,4}=2mol\)
\(\rightarrow m_{HCl}=2.36,5=73g\)
\(\rightarrow C\%_{HCl}=\frac{73.100}{73+327}=18,25\%\)
b. \(n_{CaCO_3}=\frac{50}{100}=0,5mol\)
\(n_{HCl}=\frac{250.18,25\%}{36,25}=1,25mol\)
PTHH: \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
Từ phương trình \(n_{CaCl_2}=n_{CO_2}=0,5mol\)
\(n_{HCl\text{pứ}}=0,5.2=1mol\)
\(\rightarrow n_{HCl\text{dư}}=1,25-1=0,25mol\)
\(n_{ddsaupu}=50+250-0,5.44=278g\)
\(\rightarrow C\%_{CaCl_2}=\frac{0,5.111.100}{278}=19,96\%\)
\(\rightarrow C\%_{HCl}=\frac{0,25.36,5.100}{278}=3,28\%\)

Bài 1 (SGK trang 76)
Hãy chọn câu đúng :
A. Phi kim dẫn điện tốt.
B. Phi kim dẫn nhiệt tốt.
C. Phi kim chỉ tồn tại ở hai trạng thái rắn, khí.
D. Phi kim dẫn điện, dẫn nhiệt kém.

a) Có chất rắn màu đỏ bám vào bề mặt kẽm, màu xanh của dung dịch nhạt dần:
CuCl2 (dd) + Zn(r) -> ZnCl2(dd) + Cu(r)
b) Chất rắn màu trắng bám vào bề mặt đồng. Đồng đẩy được Ag ra khỏi dung dịch muối, màu xanh lam xuất hiện trong dung dịch
Cu +2 Ag NO3 ------ > Cu( NO3)2 + 2Ag \(\downarrow\)
c) Không có hiện tượng xảy ra và không có phản ứng.
d) Có chất rắn màu đỏ bám vào bề mặt nhôm, màu xanh của dung dịch nhạt dần.
2Al(r) + 3CuCl2(dd) -> 2AlCl3 + Cu(r)
Xanh đỏ
Hiện tượng xảy ra:
a) Có chất rắn màu đỏ bám vào bề mặt kẽm, màu xanh của dung dịch nhạt dần.
CuSO4 + Zn → ZnSO4 + Cu ↓
b) Chất rắn màu trắng bám vào bề mặt đồng. Đồng đẩy được Ag ra khỏi dung dịch muối, màu xanh lam xuất hiện trong dung dịch.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
c) Không có hiện tượng gì xảy ra và không có phản ứng.
d) Có chất rắn màu đỏ bám vào bề mặt nhôm, màu xanh dung dịch nhạt dần.
2Al + 3CuCl2 → 2AlCl3 + 3Cu ↓
Bạn chia nhỏ câu hỏi ra nhé.