Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.
KN03 --> KN02 + 1/2 02
b.
n 02 = 0,075 mol
mà H% đạt 85%
=> n 02 lí thuyết thu đc = 0,075*100/85 = 3/34 mol
KN03 --> KN02 + 1/2 02
3/17 mol <---- 3/34 mol
vậy n KN03 = 3/17 mol
c.
n KN03 = 0,1
KN03 ---> KN02 + 1/2 02
lí thuyết:..0,1 -----------------> 0,05
mà H% = 80%
=> n 02 thu được = 0,05*80/100 = 0,04 mol
=> V 02 thực tế thu dc = 0,896 lit

Hướng dẫn: câu a, lập phương trình tự làm nha
b, có 6,4 g O2 thì tính được mol O2, theo phương trình tính được mol KNO3 rồi tính được khối lượng KNO3. mKNO3(thực tế)=mKNO3(tính theo PTHH)x100/H
c, tương tự câu b nhưng mO2(thực tế)=mO2(lý thuyết)xH/100
a. PTHH: \(2KNO_3\rightarrow2KNO_2+O_2\)
b. \(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\)
Theo PT ta có: \(n_{KNO_3\left(theoPT\right)}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
\(n_{KNO_3\left(thực-tế\right)}=0,4:85\%=\dfrac{8}{17}\left(mol\right)\)
=> \(m_{KNO_3\left(thực-tế\right)}=\dfrac{8}{17}.101\approx47,53\left(g\right)\)
c. \(n_{KNO_3}=\dfrac{20,2}{101}=0,2\left(mol\right)\)
=> \(n_{KNO_3\left(pư\right)}=0,2.80\%=0,16\left(mol\right)\)
=> \(n_{O_2}=\dfrac{0,16.1}{2}=0,08\left(mol\right)\)
=> \(V_{O_2}=0,08.22,4=1,792\left(l\right)\)

\(n_{O_2}=\dfrac{0,64}{32}=0,02mol\\ 2KNO_3\xrightarrow[]{t^0}2KNO_2+O_2\\ n_{KNO_3\left(lí.thuyết\right)}=0,02.2=0,04mol\\ n_{KNO_3\left(thực.tế\right)}=0,04:80\%=0,05mol\\ m_{KNO_3\left(cần\right)}=0,05.101=5,05g\\ \Rightarrow B\)

a) \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
Phản ứng phân hủy
b) \(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
PTHH: 2KNO3 --to--> 2KNO2 + O2
0,15<--------------------0,075
=> \(m_{KNO_3\left(PTHH\right)}=0,15.101=15,15\left(g\right)\)
=> mKNO3 (thực tế) = \(\dfrac{15,15.100}{85}=17,824\left(g\right)\)
c) \(n_{KNO_3\left(pư\right)}=\dfrac{10,1.80\%}{101}=0,08\left(mol\right)\)
=> nO2 = 0,04 (mol)
=> VO2 = 0,04.22,4 = 0,896(l)

a) PTHH: 2KNO3 -> (t°) 2KNO2 + O2
b) nKNO3 = 35,35/101 = 0,35 (mol)
nKNO2 = nKNO3 = 0,35 (mol)
mKNO2 = 0,35 . 85 = 29,75 (g)
c) nKNO3 = 40,4/101 = 0,4 (mol)
nO2(LT) = 0,4/2 = 0,2 (mol)
nO2(TT) = 0,2 . 75% = 0,15 (mol)
VO2 = 0,15 . 22,4 = 3,36 (l)

Theo Đề bài ta có :
PTHH :
2KNO3 -----> 2KNO2 + O2
Ta có :
nO2 = 2,4 : 32 = 0,075(mol)
=> nO2(lý Thuyết) = 0,075:85% = 0,088(mol)
=> nKNO3(PU) = 0,088 . 2 = 0,176(mol)
=> mKNO3(PƯ) = 17,78(g)
c)
nKNO3 = 10,1 : (39 + 14 + 48) = 0,1(mol)
=> nKNO3(PƯ) = 0,1 . 80% = 0,08(mol)
=> nO2 = 0,04(mol)
=> mO2 = 0,04 . 32 = 1,28(g)
Theo đề bài ta có : \(nO2=\dfrac{2,4}{16}=0,15\left(mol\right)\)
a) PTHH :
\(2KNO3-^{t0}\rightarrow2KNO2+O2\)
0,3 mol..................................0,15mol
b) Khối lượng của KNO3 cần dùng là : \(mKNO3=\dfrac{\left(0,3.101\right).85}{100}=25,755\left(g\right)\)
c) Theo đề bài ta có : nKNO3 = \(\dfrac{10,1}{101}=0,1\left(mol\right)\)
khối lượng khí oxi điều chế được khi phân huỷ là : \(mO2=\dfrac{\left(0,1.32\right).80}{100}=2,56\left(g\right)\)

a) PTHH:
2KNO3→2KNO2 + O2
b)\(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)Theo PTHH ta có:
nKNO3=2nO2=0,15(mol)
mKNO3 ban đầu=0,15.101=15,15(g)
mKNO3 thực tế=15,15.\(\dfrac{85}{100}\)=12,8775(g)

a, PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b, Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Theo PT: \(n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{30}\left(mol\right)\Rightarrow m_{Fe_3O_4}=\dfrac{1}{30}.232\approx7,733\left(g\right)\)
c, Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}=\dfrac{1}{15}\left(mol\right)\)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4\left(LT\right)}=2n_{O_2}=\dfrac{2}{15}\left(mol\right)\)
\(\Rightarrow m_{KMnO_4\left(LT\right)}=\dfrac{2}{15}.158=\dfrac{316}{15}\left(g\right)\)
Mà: H% = 85%
\(\Rightarrow m_{KMnO_4\left(TT\right)}=\dfrac{\dfrac{316}{15}}{85\%}\approx24,78\left(g\right)\)

PTHH: 2KNO3 =(nhiệt)=> 2KNO2 + O2
Ta có: nO2 = \(\frac{6,4}{32}=0,2\left(mol\right)\)
=> nKNO3(theo phương trình) = 0,4 (mol)
=> nKNO3(thực tế) = \(0,4\div\frac{85}{100}=\frac{8}{17}\left(mol\right)\)
=> mKNO3(thực tế) = \(\frac{8}{17}\times101=47,53\left(gam\right)\)
Ta có:
\(PTHH:2KNO_3->>2KNO_2+O_2\)
Ta có:
\(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{6,4}{32}=0,2\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_{KNO_3}=2.n_{O_2}=2.0,2=0,4\left(mol\right)\)
Theo thực tế, ta được:
\(n_{KNO_3\left(thựctế\right)}=0,4:85\%=\frac{8}{17}\left(mol\right)\)
Khối lượng KNO3 trong thực tế:
\(m_{KNO_3\left(thựctế\right)}=n_{KNO_3}.M_{KNO_3}=\frac{8}{17}.101\approx47,529\left(g\right)\)
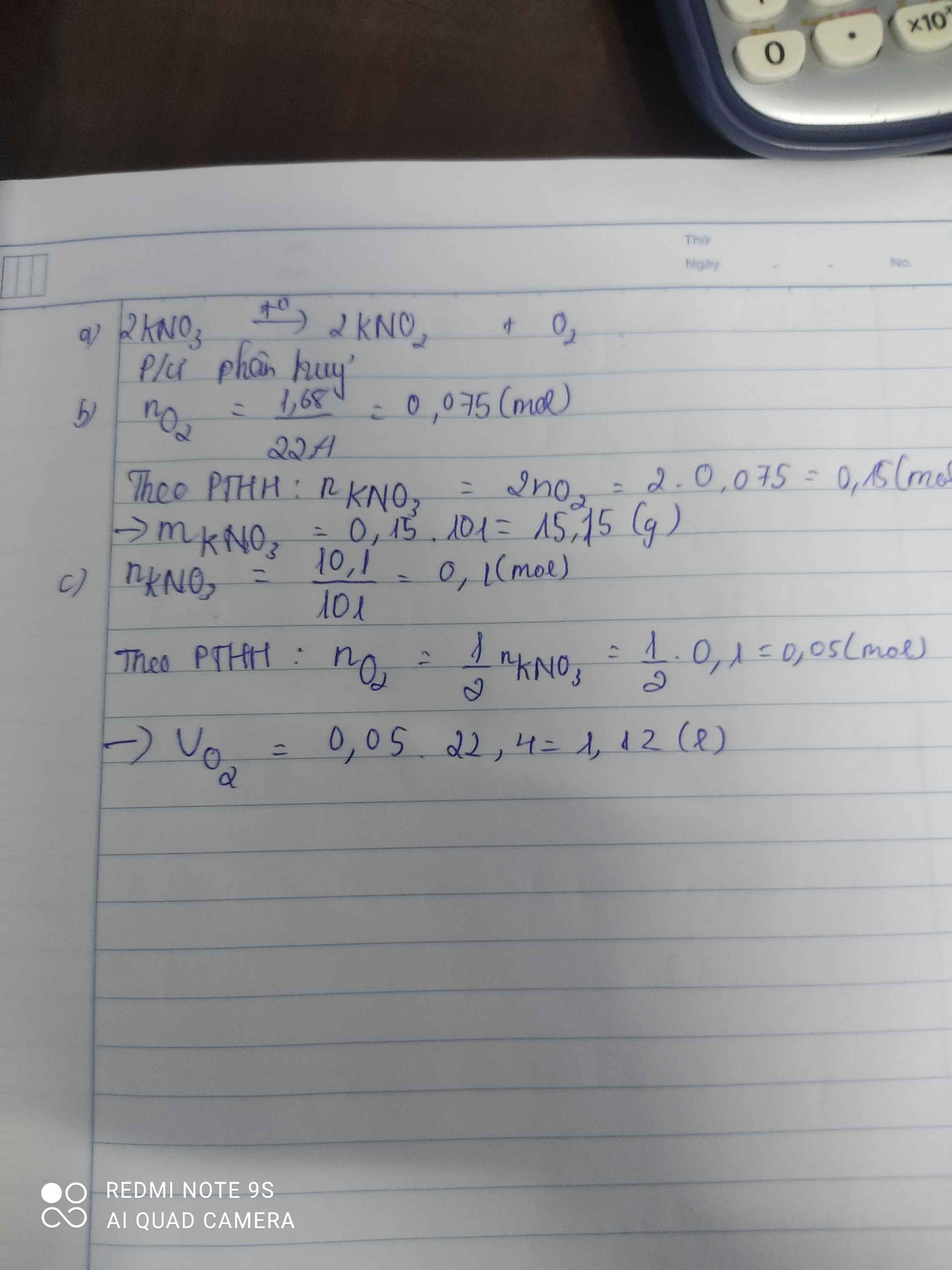
2KNO3\(\rightarrow\)2KNO2 + O2
b;nO2=\(\dfrac{2,4}{32}=0,075\left(mol\right)\)
Theo PTHH ta có:
nKNO3=2nO2=0,15(mol)
mKNO3 ban đầu=0,15.101=15,15(g)
mKNO3 thực tế=15,15.\(\dfrac{85}{100}=12,8775\left(g\right)\)
c;
nKNO3=\(\dfrac{10,1}{101}=0,1\left(mol\right)\)
Theo PTHH ta có:
\(\dfrac{1}{2}\)nKNO3=nO2=0,05(mol)
mO2 ban đầu=32.0,05=1,6(g)
mO2 thu được=1,6\(\dfrac{85}{100}=1,36\left(g\right)\)
dạ cảm ơn ạ