Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
n(CO32–) = 0,2 mol; n(HCO3–) = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32– và HCO32– đã phản ứng
→ n(H+) = 2x.2 + 3x = 0,42 => x = 0,06 → n(CO2) = 2x + 3x = 0,3 mol.
Có n(OH–) = 0,36
Xét tỉ lệ T = n(OH–) / n(CO2) thấy tạo ra đồng thời 2 muối CO32– và HCO3–.
→ n(CO32–) = 0,06; n(HCO3–) = 0,24
n(Ba2+) = 0,08 → n(BaCO3) = 0,06 → m(BaCO3) = 11,82 gam.

Đáp án C
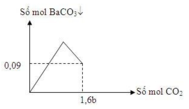
Cho 1,6b mol CO2 vào b mol Ba(OH)2 thu được 0,09 mol kết tủa BaCO3.
n B a C O 3 = 2b - 1,6b = 0,09 => b = 0,225 → n C O 2 = 1,6b = 0,36 mol
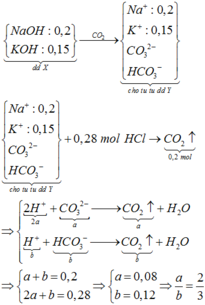
Rót từ từ dung dịch X vào HCl thì các muối trong X phản ứng theo tỉ lệ mol:
![]()
![]()
Vậy dung dịch Y chứa 0,2 mol Na2CO3 dư, 0,4 mol NaHCO3 dư và NaCl 0,48 mol
→ m C T = 82 , 88 g a m

Giải thích:
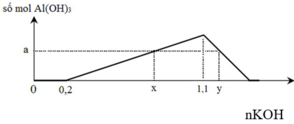
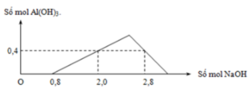
Tại nNaOH = 0,8 mol thì bắt đầu có kết tủa xuất hiện
⇒ H+ trung hòa vừa hết ⇒ nHCl = a = 0,8 mol
Tại nNaOH = 2,0 và 2,8 mol thì cùng thu được lượng kết tủa như nhau
+) nNaOH = 2,0 mol thì Al3+ dư
+) nNaOH = 2,8 mol thì kết tủa tan 1 phần:
nAl(OH)3 = 4nAl3+−(nOH − nHCl) ⇒ nAlCl3 = b = 0,6 mol
Đáp án B

Đáp án A
♦ YTHH 03: sinh 0,14 mol H2 ||→ thêm 0,14 mol O vào 40,1 gam hỗn hợp
chuyển về 42,34 gam chỉ gồm oxit Na2O và BaO; từ 0,28 mol NaOH → có 0,14 mol Na2O
||→ có 0,22 mol BaO → đọc ra 0,22 mol Ba(OH)2 ||→ X chứa 0,72 mol OH–.
Phản ứng: 2OH– + CO2 → CO32– + H2O || OH– + CO2 → HCO3–.
biết nCO2 = 0,46 mol ||→ sau phản ứng có: 0,26 mol CO22– và 0,2 mol HCO3–.
0,22 mol Ba2+ và 0,28 mol Na+ ||→ đọc ra Y gồm: 0,04 mol Na2CO3 và 0,2 mol NaHCO3.
Mặt khác, 200 ml dung dịch Z gồm (0,08 + y) mol H+ ||→ a = 2,5y là giá trị cần tìm.
► giải theo trắc nghiệm: chọn TH khó nhất để giải (tự luận sẽ phải chặt chẽ hơn, xét thêm TH).
♦ cho H+ từ từ vào Y: H+ + CO3– → HCO3– trước, sau đó: H+ + HCO3– → CO2↑ + H2O.
DỰa vào số liệu → nCO2 = (0,08 + y) – 0,04 = x (1).
♦ Cho ngược lại: xảy ra đồng thời: HCO3– + H+ → CO2 + H2O || CO32– + 2H+ → CO2 + H2O.
giả sử có z mol CO32– phản ứng thì tương ứng có 5z mol HCO3– phản ứng (tỉ lệ 0,04 ÷ 0,2 = 1 ÷ 5)
||→ ∑nkhí CO2 = z + 5z = 1,2x và ∑nH+ = 2z + 5z = 7z = 0,08 + y ||→ 1,4x = 7z = 0,08 + y (2).
Giải (1) và (2) ||→ x = 0,1 mol và y = 0,06 mol ||→ a = 2,5y = 0,15.
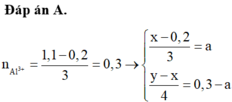
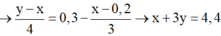
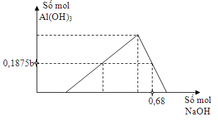


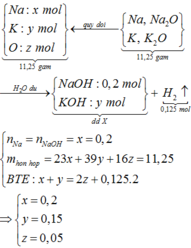
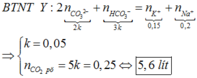
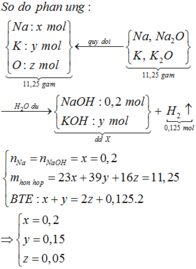
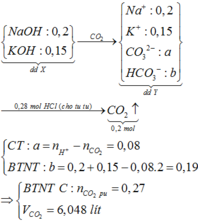
Chọn đáp án A
nNaOH = 0,08 (mol) ; nK2CO3 = 0,06 (mol)
Nhỏ rất từ từ HCl vào dd NaOH và K2CO3 sẽ có phản ứng theo thứ tự:
H+ + OH- → H2O (1)
0,08 ← 0,08
H+ + CO32- → HCO3- (2)
0,06←0,06
H+ + HCO3- → CO2↑+ H2O(3)
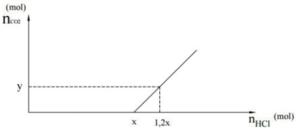
Nhìn đồ thị ta thấy: giai đoạn bắt đầu xuất hiện khí thoát ra => nHCl = x (mol)
=> Lượng HCl này chính là lượng phản ứng ở (1) và (2)
=> x = 0,08 + 0,06 = 0,14 (mol)
Khí bắt đầu thoát ra đến khi nHCl = 1,2x (mol)
=> khi này phương trình (3) bắt đầu xảy ra
=> theo (3) nCO2 thoát ra = nHCl pư (3)
= (1,2x –x) = 0,2x = 0,2.0,14
= 0,028 (mol)