Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol CaCO3, MgCO3 là a, b (mol)
=> 100a + 84b = 14,2 (1)
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
a-------------------->a
MgCO3 --to--> MgO + CO2
b---------------------->b
=> a + b = 0,15
=> a = 0,1; b = 0,05
=> \(\left\{{}\begin{matrix}\%m_{CaCO_3}=\dfrac{100.0,1}{14,2}.100\%=70,42\%\\\%m_{MgCO_3}=\dfrac{0,05.84}{14,2}.100\%=29,58\%\end{matrix}\right.\)
\(n_{CO_2}=\dfrac{6,6}{44}=0,15mol\)
\(CaCO_3\underrightarrow{t^o}CO_2+CaO\)
\(x\) \(\rightarrow\) \(x\)
\(MgCO_3\underrightarrow{t^o}MgO+CO_2\)
\(y\) \(\rightarrow\) \(y\)
\(\Rightarrow\left\{{}\begin{matrix}100x+84y=14,2\\x+y=0,15\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,1\cdot100}{14,2}\cdot100\%=70,42\%\)
\(\%m_{MgCO_3}=100\%-70,42\%=29,57\%\)

Theo định luật bảo toàn khối lượng, ta có khối lượng khí oxi thu được là:
m O 2 = 24,5 – 13,45 = 11,05(g)
Khối lượng thực tế oxi thu được: m O 2 = (11,05 x 80)/100 = 8,84 (g)

\(m_{CaCO_3}=90\%.400=360\left(g\right)\\ \rightarrow n_{CaCO_3}=\dfrac{360}{100}=3,6\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
3,6 ----------> 3,6 -----> 3,6
\(\rightarrow n_{CaO}=3,6.75\%=2,7\left(mol\right)\\ \rightarrow n_{CaCO_3\left(chưa.pư\right)}=3,6-2,7=0,9\left(mol\right)\)
\(\rightarrow m_X=0,9.100+2,7.56=241,2\left(g\right)\\ \%m_{CaO}=\dfrac{0,9.100}{241,2}=37,31\%\)
\(V_Y=V_{CO_2}=3,6.75\%.22,4=60,48\left(l\right)\)
\(m_{CaCO_3}=\dfrac{400\cdot90\%}{100\%}=360g\Rightarrow n_{CaCO_3}=\dfrac{360}{100}=3,6mol\)
\(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
3,6 3,6 3,6
Thực tế: \(n_{CaO}=3,6\cdot75\%=2,7mol\)
\(\Rightarrow m_{CaO}=2,7\cdot56=151,2g\)

\(m_{CaCO_3}=400\cdot90\%=360\left(g\right)\)
\(m_{trơ}=400-360=40\left(g\right)\)
\(n_{CaCO_3}=\dfrac{360}{100}=3.6\left(mol\right)\)
\(a.\)
\(n_{CaCO_3\left(pư\right)}=3.6\cdot75\%=2.7\left(mol\right)\)
\(CaCO_3\underrightarrow{^{^{t^0}}}CaO+CO_2\)
\(2.7........2.7...........2.7\)
\(m_X=m_{CaO}+m_{CaCO_3\left(dư\right)}+m_{trơ}=2.7\cdot56+\left(3.6-2.7\right)\cdot100+40=281.2\left(g\right)\)
\(b.\)
\(\%CaO=\dfrac{2.7\cdot56}{281.2}\cdot100\%=53.77\%\)
\(V_{CO_2}=2.7\cdot22.4=60.48\left(l\right)\)

a)mCaCO3=500.80%=400(g) -> nCaCO3=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + H2O
nCaO(LT)=nCaCO3=4(mol)
=> nCaO(TT)=4. 70%=2,8(mol)
=>mX=mCaO+ m(trơ)+ mCaCO3(chưa p.ứ)=2,8.56+100+ 1,2.100=376,8(g)
b) %mCaO= (156,8/376,8).100=41,614%

mgiảm = mO (sinh ra) = 100 - 90,4 = 9,6 (g)
-> nO2 = \(\dfrac{9,6}{32}=0,3\left(mol\right)\)
PTHH: 2KClO3 \(\underrightarrow{t^o,MnO_2}\) 2KCl + 3O2
0,2 0,6
mKCl = 0,2.74,5 = 19,9 (g)
mKClO3 = 90,4 - 19,9 = 70,5 (g)
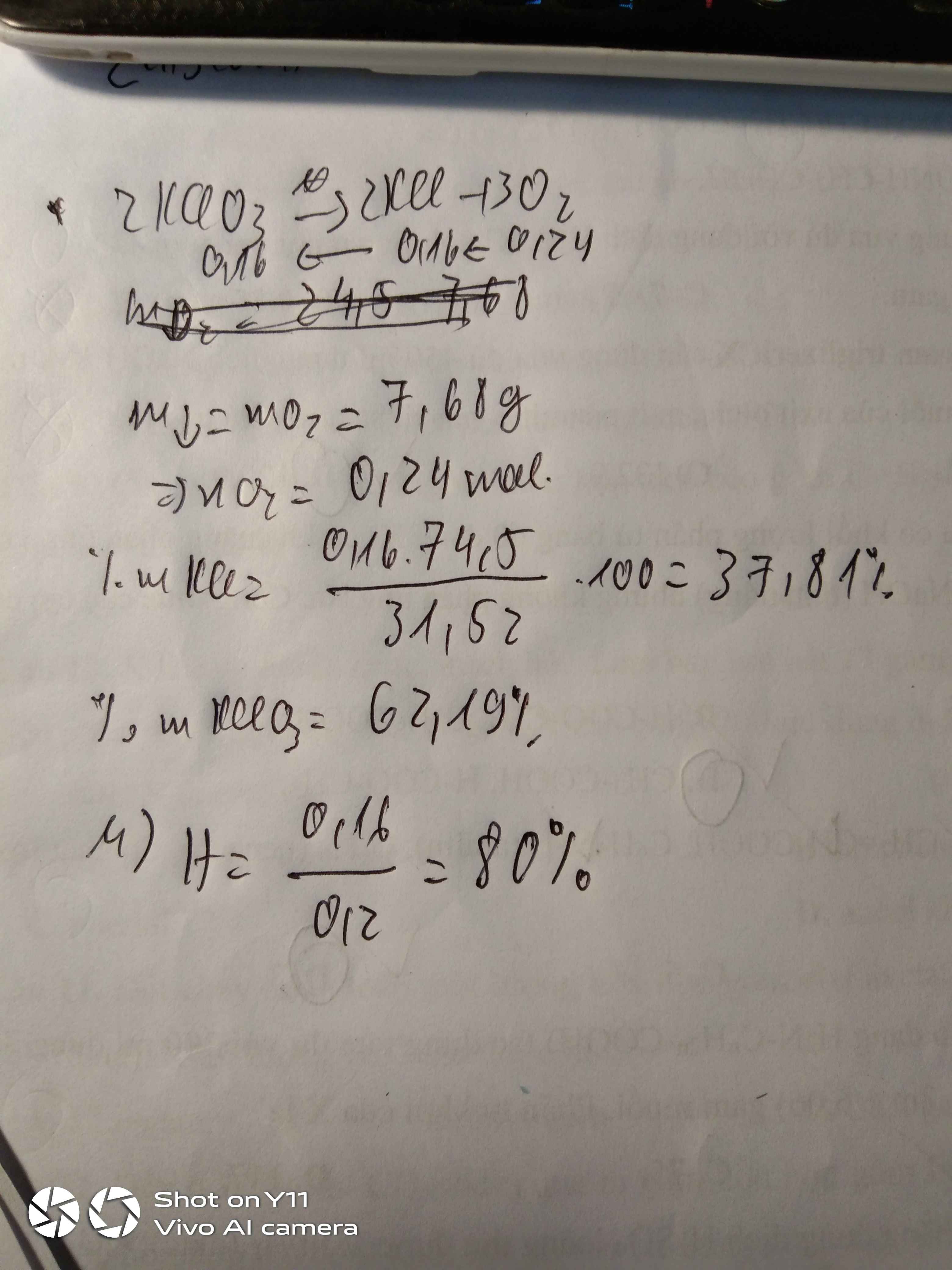
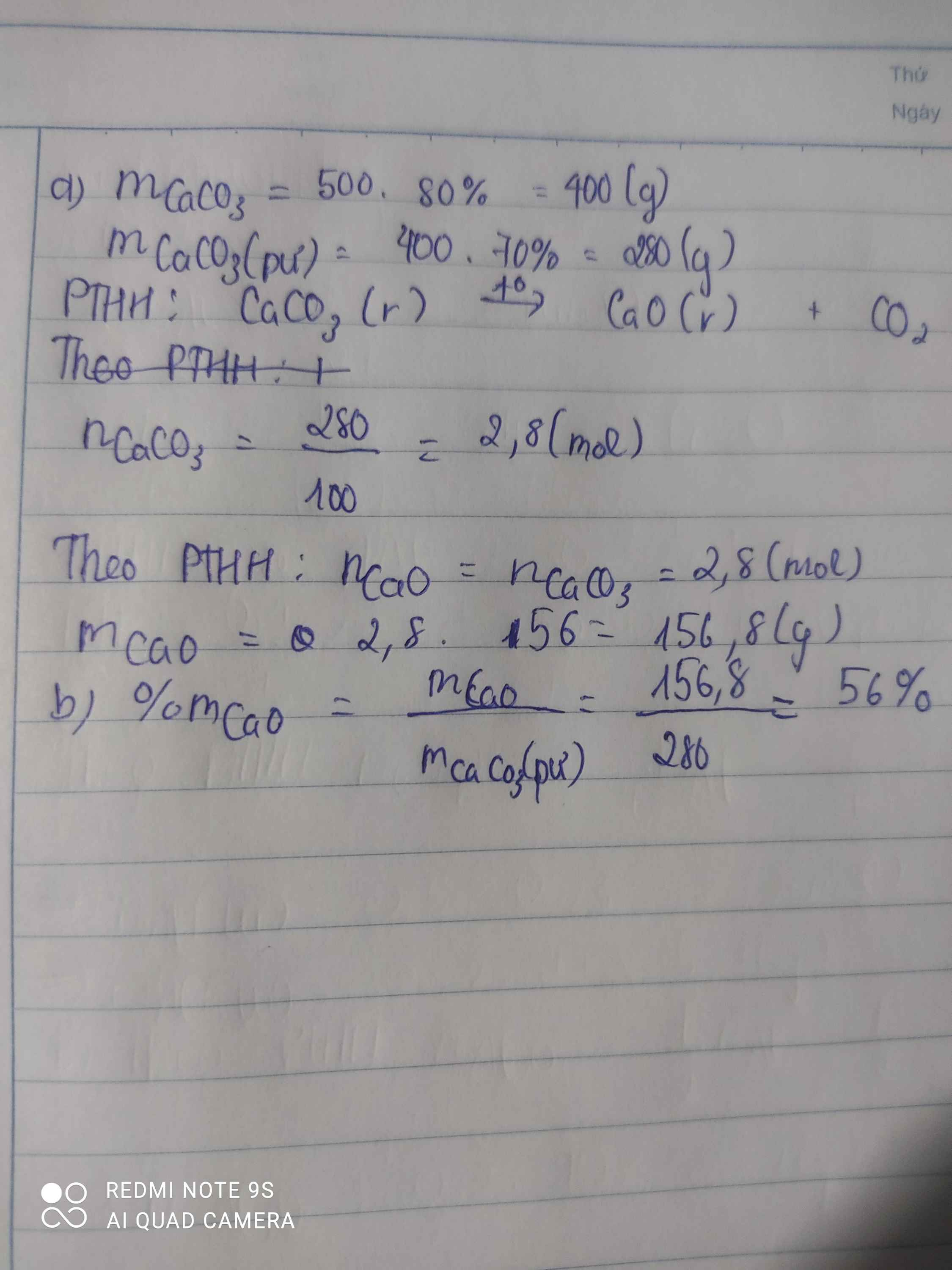
a) \(n_{MgCO_3}=\dfrac{25,2}{84}=0,3\left(mol\right)\)
PTHH: MgCO3 --to--> MgO + CO2
________a---------->a
=> 40a + 84(0,3-a) = 14,64
=> a = 0,24
=> \(H\%=\dfrac{0,24}{0,3}.100\%=80\%\)
b) mMgO = 0,24.40 = 9,6 (g)
mMgCO3 = (0,3-0,24).84 = 5,04 (g)