Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
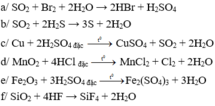
→ Các phản ứng a, b, c và d thuộc phản ứng oxi hóa – khử

\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.15.................................0.15\)
\(n_{Fe}=1.25\cdot0.15=0.1875\left(mol\right)\)
\(2Fe+6H_2SO_{4\left(đ\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(0.1875..........................................0.28125\)
\(V_{SO_2}=6.3\left(l\right)\)

Đáp án C.
Các phương trình oxi hóa khử là I, II, III, IV.
Các pt phản ứng xảy ra:
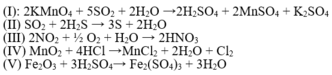

Gọi \(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
Phần 1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Fe+H_2SO_{4l}\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow n_{Fe}=0,2mol\Rightarrow m_{Fe}=0,2\cdot56=11,2g\)
Phần 2:
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(BTe:2n_{Cu}+3n_{Fe}=2n_{SO_2}=0,8\)
\(\Rightarrow n_{Cu}=\dfrac{0,8-3\cdot0,2}{2}=0,1mol\)
\(\Rightarrow m_{Cu}=0,1\cdot64=6,4g\)
Vậy \(m_X=m_{Cu}+m_{Fe}=6,4+11,2=17,6g\)

Khí SO 2 khí này làm mất màu dung dịch KMn O 4
2 H 2 SO 4 + Cu → CuS O 4 + SO 2 + 2 H 2
2 H 2 O + 2KMn O 4 + 5 SO 2 → 2 H 2 SO 4 + 2MnS O 4 + K 2 SO 4
(không màu) (tím) (không màu, mùi sốc) (không màu) (trắng)

Đáp án B
Bảo toàn e: nCu = nSO2 = 0,2 (mol)
nNaOH = 2.0,2 = 0,4 (mol)
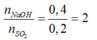
Tạo muối Na2SO3
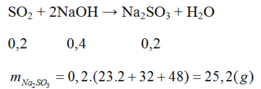


Đáp án là D. Khí sunfurơ.