Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a) n_{CuO} = \dfrac{30,3.26,4\%}{80} = 0,1(mol)\\ n_{PbO} = \dfrac{30,3-0,1.80}{223} = 0,1(mol)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ PbO + H_2 \xrightarrow{t^o} Pb + H_2O\\ n_{Cu} = n_{CuO} = 0,1(mol) \Rightarrow m_{Cu} = 0,1.64 = 6,4(gam)\\ n_{Pb} = n_{PbO} = 0,1(mol) \Rightarrow m_{Pb} = 0,1.207 = 20,7(gam)\\ b) n_{H_2O} = n_{CuO} + n_{PbO} = 0,2(mol) \Rightarrow m_{H_2O} = 0,2.18 = 3,6(gam)\\ \Rightarrow V_{H_2O} = \dfrac{3,6}{1} = 3,6(ml)\)

\(a) CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ b) n_{CuO} = \dfrac{32.25\%}{80} = 0,1(mol)\\ n_{Fe_2O_3} = \dfrac{32-0,1.80}{160} = 0,15(mol)\\ n_{Cu} = n_{CuO} = 0,1(mol) \Rightarrow m_{Cu} = 0,1.64 = 6,4(gam)\\ n_{Fe} = 2n_{Fe_2O_3} = 0,3(mol) \Rightarrow m_{Fe} = 0,3.56 = 16,8(gam)\)

a)
\(CuO + H_2\xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O\\ Fe + 2HCl \to FeCl_2 + H_2\\ b) n_{Fe} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ \Rightarrow m_{Cu} = \dfrac{12-0,1,56}{64}=0,1(mol)\\ n_{Fe_2O_3} = \dfrac{n_{Fe}}{2} = 0,05(mol)\\ n_{CuO} = n_{Cu} = 0,1(mol)\\ \%m_{Fe_2O_3} =\dfrac{0,05.160}{0,05.160 + 0,1.80}.100\% = 50\%\\ \%m_{CuO} = 50\%\)
\(c) n_{H_2} = 3n_{Fe_2O_3} + n_{CuO} = 0,05.3 + 0,1 = 0,25(mol)\\ V_{H_2} = 0,25.22,4 = 5,6(lít)\)
\(d) n_{H_2O} = n_{H_2} = 0,25(mol)\\ m_{H_2O} = 0,25.18 = 4,5(gam)\)

\(Đặt:n_{CuO}=a\left(mol\right);n_{PbO}=b\left(mol\right)\left(a,b>0\right)\\ n_{H_2O}=\dfrac{1,35}{18}=0,075\left(mol\right)\\ CuO+H_2\underrightarrow{^{to}}Cu+H_2O\\ PbO+H_2\underrightarrow{^{to}}Pb+H_2O\\ \Rightarrow\left\{{}\begin{matrix}80a+223b=8,145\\a+b=0,075\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,06\\b=0,015\end{matrix}\right.\\ \Rightarrow\%m_{CuO}=\dfrac{0,06.80}{8,145}.100\approx58,932\%\\ \Rightarrow\%_{PbO}\approx41,068\%\)

a) \(m_{CuO}=\dfrac{20.40}{100}=8\left(g\right)\) => \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(m_{Fe_2O_3}=20-8=12\left(g\right)\) => \(n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,1--->0,1------>0,1
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,075--->0,225----->0,15
=> mCu = 0,1.64 = 6,4 (g)
=> mFe = 0,15.56 = 8,4 (g)
b) \(V_{H_2}=\left(0,1+0,225\right).22,4=7,28\left(l\right)\)

PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
a, Ta có: \(\left\{{}\begin{matrix}m_{Fe_2O_3}=20.60\%=12\left(g\right)\Rightarrow n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\\m_{CuO}=20-12=8\left(g\right)\Rightarrow n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\end{matrix}\right.\)
Theo pT: \(\left\{{}\begin{matrix}n_{Fe}=2n_{Fe_2O_3}=0,15\left(mol\right)\\n_{Cu}=n_{CuO}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
b, Theo PT: \(n_{H_2}=3n_{Fe_2O_3}+n_{CuO}=0,325\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,325.22,4=7,28\left(l\right)\)
Bạn tham khảo nhé!

\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\\ CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\\ Đặt:n_{Fe_2O_3}=a\left(mol\right);n_{CuO}=b\left(mol\right)\left(a,b>0\right)\\ m_{hhoxit}=k\left(g\right)\\ \Rightarrow\left(1\right)160a+80b=k\\ \left(2\right)112a+64b=0,72k\\ \Rightarrow6,4a=12,8b\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{12,8}{6,4}=\dfrac{2}{1}\\ \Rightarrow\%m_{Fe_2O_3}=\dfrac{160.2}{160.2+80.1}.100=80\%\\ \Rightarrow\%m_{CuO}=20\%\)

1)
Phần trăm O trong oxit là 100% -76% = 24%
$CO + O_{oxit} \to CO_2$
Ta thấy :
m khí tăng = m O(oxit) = 9,6(gam)
=> m1 = 9,6/24% = 40(gam)
n O(oxit) = 9,6/16 = 0,6(mol)
Bảo toàn khối lượng :
m kim loại = m oxit - m O = 40 - 0,6.16 = 30,4(gam)
$Fe + 2HCl \to FeCl_2 + H_2$
n Fe = n H2 = 4,48/22,4 = 0,2(mol)
=> m Cu = m 2 = 30,4 - 0,2.56 = 19,2(gam)
b)
n CuO = n Cu = 19,2/64 = 0,3(mol)
Ta có :
n O(trong oxit sắt) = n O(oxit) - n O(trong CuO) = 0,6 -0,3 = 0,3(mol)
Ta thấy :
n Fe : n O = 0,2 : 0,3 = 2 : 3
Vậy oxit cần tìm là Fe2O3

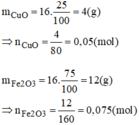
PTHH của phản ứng là:
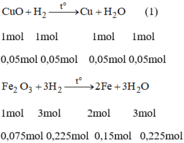
Từ pt (1), ta có: n C u = n C u O = 0,05 mol
m C u = 0,05.64 = 3,2(g)
Từ pt (2), ta có n F e = 2 . n F e 2 O 3 = 2. 0,075 = 0,15 mol
m F e = 0,15.56 = 8,4(g)