Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(pH=14+log\left(OH^-\right)\) \(\Rightarrow log\left(OH^-\right)=-4\)
\(\Rightarrow\left[OH^-\right]=C_{M_{NaOH}}=0,0001\left(M\right)\)
\(\Rightarrow n_{NaOH}=0,0001\cdot0,25=2,5\cdot10^{-5}\left(mol\right)\)
\(\Rightarrow m_{NaOH}=2,5\cdot10^{-5}\cdot40=0,001\left(g\right)\)

Khi pH = 10 thì [H+] = 1.10-10M và
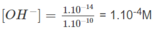
nghĩa là cần có 1. 10 - 4 mol NaOH trong 1 lít dung dịch.
Vậy trong 250 ml (0,25 lít) dung dịch cần có 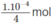 NaOH hoà tan, nghĩa là cần có
NaOH hoà tan, nghĩa là cần có
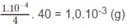 NaOH
NaOH

\(pH=14+log\left[OH^-\right]=10\)
\(\Rightarrow\left[OH^-\right]=10^{-4}\)
\(n_{NaOH}=10^{-4}\cdot0.3=3\cdot10^{-5}\left(mol\right)\)
\(m_{NaOH}=3\cdot10^{-5}\cdot40=1.2\cdot10^{-3}\left(g\right)\)

Câu 1 :
Gọi thể tích dung dịch ban đầu là V(lít)
$[H^+] = 10^{-3}V(mol)$
Thể tích dung dịch lúc sau là :
$V' = \dfrac{10^{-3}.V}{10^{-4}} = 10V$
Do đó cần pha loãng dung dịch ban đầu 10 lần thì thu được dung dịch trên

Đáp án D
Gọi thể tích dung dịch NaOH ban đầu là V
Gọi thể tích dung dịch NaOH sau khi pha là V1
Ta có số mol NaOH ko đổi nên
V.10-3 = V1. 10-5 suy ra V1 = 100V tức là pha loãng 100 lần



cần thêm 1 lượng nước có thể tích bằng 9 lần thể tích dd ban đầu
[OH-] giảm đi 10 lần
mà nOH- không đổi
Vsau=10Vđầu
V nước thêm vào=Vsau-Vđầu=9Vđầu
pH=10
=>pOH=4
=>[OH]=10^-4
=>[NaOH]=10^-4 M
=>nNaOH=3*10^-5
=>mNaOH=0,00069g
1,2*10^-3