Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có sơ đồ phản ứng: ( C 6 H 10 O 5 ) → 2 n C 2 H 5 O H
Theo phương trình:
n ( C 6 H 10 O 5 ) n = 8 2 n → m ( C 6 H 10 O 5 ) n = 8 2 n . 162 n = 648 g a m
M à H = 80 % → m ( C 6 H 10 O 5 ) n = 648 80 % = 810 g a m . → a = 810 40 % = 2025 g a m

Đáp án C
Hướng dẫn
Với H = 64,8 % thì số mol của C2H5OH thu được là :

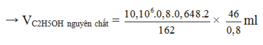
Vậy thể tích dung dịch cồn thực phẩm 40 0 thu được
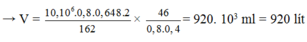

Đáp án: C
Với H = 64,8 % thì số mol của C2H5OH thu được là :


Đáp án C
Các phương trình điều chế HNO3 từ NH3
4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
2NO + O2→2NO2
4NO2 + O2 + 2H2O→ 4HNO3
Theo bảo toàn nguyên tố N ta có:
nHNO3=nNH3=112 000/22,4=5000 mol
→mHNO3=315 000 gam= 315 kg
→ mddHNO3= 315.100/60=525 kg
Do hiệu suất bằng 80% nên mddHNO3 thực = mPT.80/100= 525.80/100=420 kg

Đáp án D
PTHH : Ca3(PO4)2 → 2H3PO4
nCa3(PO4)2 =5299.0,78:310=13,33 mol → nH3PO4 = 13,33.0,75.2.0,005=0,1 mol
Các phương trình có thể xảy ra là : H3PO4 + 3NaOH → Na3PO4 + 3H2O
H3PO4 + 2NaOH → Na2 HPO4 + 2H2O
H3PO4 + NaOH → NaH2PO4 + H2O
Nếu chất rắn chỉ có muối
Lượng muối tạo ra tối đa khi tạo thành Na3PO4 => mNa3PO4 = 0,1.164 =16,4 < 17,2 → còn dư NaOH
→ chỉ tạo muối Na3PO4: 0,1 mol và còn dư NaOH : 0,8g hay 0,02 mol
Bảo toàn nguyên tố Na có 0,1.3 + 0,02 = nNaOH = 0,32 =0,1x → x =3,2M
Đáp án D
Chú ý:
Chỉ 0,05% lượng axit được tạo ra mới tham gia phản ứng với NaOH

Chọn đáp án B
Ta có 6,2 kg = 6200 g
+ Ta có 1P → 1H3PO4.
⇒ nH3PO4 = nP × 0,8
= 6200 × 0,8 ÷ 31
= 160 mol.
⇒ VH3PO4 = 160 ÷ 2 = 80 lít
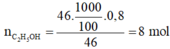
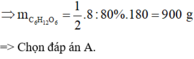

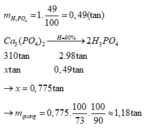
Đáp án: A
Ta có sơ đồ phản ứng: (C6H10O5) → 2nC2H5OH
Theo phương trình:
Mà H = 80% → m(C6H10O5)n = 648 : 80% = 810 gam.
→ a = 810 : 40% = 2025 gam