Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt công thức hóa học của loại thủy tinh này là:
x Na 2 O .yCaO.z SiO 2 ; M Na 2 O = 62g; M CaO = 56g; M SiO 2 = 60g
Với những điều kiện như sau : x, y, z là những số nguyên, dương ;
Tỉ lệ x : y : z là nhữiig số nguyên đơn giản nhất. Theo đầu bài ta có tí lệ :
x:y:z = 13/62 : 12/56 : 75/60 = 0,21 : 0,21 : 1,25 = 1 : 1 : 6
Công thức hóa học của loại thủy tinh trên là : Na 2 O .CaO.6 SiO 2

Gọi công thức hợp chất: xCaO.yNa2O.zSiO2
Tỉ lệ x: y: z = 12/56:13/62:75/60 = 0,21: 0,21: 1,25 = 1: 1: 6
Công thức hóa học ở dạng oxit của chất đó: CaO.Na2O.6SiO2

(a) Phản ứng nổ của TNT: 2C7H5N3O6 → 3N2 + 5H2O + 7CO + 7C
(b) 100 gam thuốc nổ Hexanit có chứa 60 gam TNT và 40 gam HND.
Số mol của từng chất là:
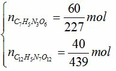
Áp dụng định luật bảo toàn nguyên tố ta có:
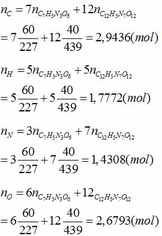
- Phần trăm khối lượng mỗi nguyên tố trong Hexanit:
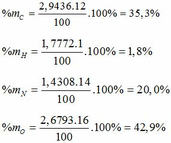
- Sản phẩm nổ của Hexanit là N2, H2O, CO, C
- Áp dụng định luật bảo toàn nguyên tố ta tính được số mol của các chất trong hỗn hợp sau khi nổ:
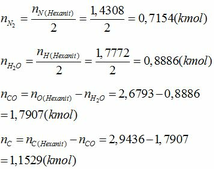
Phần trăm số mol của các chất trong hỗn hợp sau khi nổ:
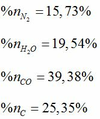

Gọi cthh của oxit là AxOy (x,y là số tự nhiên > 0)
Ta có: \(\dfrac{x.M_A}{y.16}=\dfrac{9}{8}\Leftrightarrow18y=x.M_A\)
TH1: CTHH của oxit là trường hợp đặc biệt Fe3O4
=> \(\dfrac{m_{Fe}}{m_O}=\dfrac{3.56}{4.16}=\dfrac{21}{8}\left(L\right)\)
TH2: CTHH của oxit là A2Oy
=> 9y =MA => y = 3, MA = 27(g/mol) => A là nhôm (Al)
CTHH của oxit là Al2O3




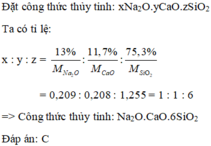
Gọi công thức thủy tinh là xNa2O.yCaO.zSiO2
\(x:y:z=\dfrac{12,97}{62}:\dfrac{11,72}{56}:\dfrac{75,31}{60}=1:1:6\)
Loại thủy tinh này có dạng Na2O.CaO.6SiO2